[化学—选修3:物质结构与性质]
在元素周期表中,除稀有气体外几乎所有元素都能氢形成氢化物。
(1)氨气属于共价型氢化物,工业常用氨气和醋酸二氨合铜[Cu(NH3)2]Ac的混合液来吸收一氧化碳(醋酸根CH3COO-简写为Ac-)。反应方程式为:[Cu(NH3)2]Ac+CO+NH3═[Cu(NH3)3CO]Ac
①请写出基态Cu+离子的价电子排布式_________________。
②氨水溶液中各元素原子的第一电离能从大到小排列顺序为_______________,理由是_________;其中NH3应为_________(填“极性”或“非极性”)分子。
③醋酸分子(CH3COOH)中的两个碳原子的杂化方式分别是_________________。
④生成物[Cu(NH3)3CO]Ac中所含化学键类型有_________(填序号)。
a.离子键 b.金属键 c.共价键 d.配位键
(2)某离子型氢化物化学式为XY2,晶胞结构如图所示,其中6个Y原子(○)用阿拉伯数字1~6标注.
①已知1、2、3、4号Y原子在晶胞上、下面上.则5、6号Y原子均在晶胞_________(填“侧面”或“内部”)。
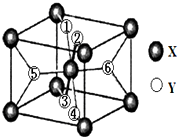
②根据以上信息可以推知,XY2晶体的熔沸点___________(填“>”“=”或“<”)固态氨的熔沸点。
③若该晶胞的边长为anm,密度为ρg/cm3,XY2的摩尔质量为Mg/mol,则阿伏加德罗常数为___________。
(1)补充完成下表:(请把序号①一④的答案对应填入答题卡上)
| 元素 |
甲 |
乙 |
丙 |
| 元素符号 |
① |
② |
O |
| 原子结构示意图 |
 |
③ |
 |
| 周期 |
三 |
三 |
二 |
| 族 |
IA |
ⅦA |
④ |
(2)甲元素最高价氧化物对应的水化物呈性(填“酸、碱”),乙元素对应的最高价氧化物的水化物化学式为。
(3)将乙单质通入到KI溶液中,发生反应的离子方程式为:_______________,向反应后的溶液中加入CCl4、震荡,溶液分层,CCl4层呈________色。
元素周期表是学习化学的重要工具,它隐含许多信息和规律,以下为周期表中1~18号元素
| a |
|||||||
| b |
c |
d |
e |
||||
| f |
g |
h |
i |
(1)a、b、f三元素原子半径大小关系为______>______>______(填元素符号,下同)
(2)c、d、e三元素最高正化合价大小关系为______>______>______
(3)元素h与i氢化物的稳定性强弱为______>______(填化学式)
(4)写出f最高价氧化物水化物溶液和g最高价氧化物水化物反应的离子方程式:_______________________________________。
(5)用电子式表示f和i单质形成化合物的过程:。
有A、B、C、D四种单质在一定条件下,B可以分别和A、C、D化合成甲、乙、丙;C和D可化合成丁.已知甲、乙、丙的每个分子中都含有10e-,并且甲、乙、丙、丁有以下关系。
回答下列问题:
(1)单质B的化学式________________;
(2)A+乙→甲+C反应方程式__________;
(3)若丙丁间有可能发生反应,则丙的化学式为___________;若丙丁间不可能发生反应,则丙的化学式为____________。
有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出AB2的电子式为___________。
(2)用电子式表示化合物C2D的形成过程___________________________________。
下表列出了①~⑨九种元素在周期表中的位置:
| ⅠA |
ⅧA |
||||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
||
| 2 |
② |
③ |
④ |
⑧ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑨ |
|||||
请按要求回答下列问题。
(1)元素⑤的名称是______,元素⑤在周期表中所处位置____________,从元素原子得失电子的角度看,元素⑤具有____________性(填“氧化性”或“还原性”)。
(2)按气态氢化物的稳定性由强到弱的顺序排列,⑥④⑦的氢化物稳定性:___________________(写氢化物的化学式)。
(3) ⑦、⑨ 最高价氧化物对应水化物的酸性由强到弱的顺序___________________(写化学式)。