向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0 mol•L-1的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
| A.Cu与Cu2O的物质的量之比为2:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
一定温度下,能说明可逆反应: 达到限度的是
达到限度的是
A.C的生成速率与A的消耗速率相等
B.单位时间生成n molA,同时生成3n mol B
C.A、B、C的浓度不再变化
D.A、B、C的分子数之比为1:3:2
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层 电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是
电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是
| A.X的氢化物溶于水显酸性 |
| B.Y的氧化物是离子化合物 |
| C.Z的氢化物的水溶液在空气中存放不易变质 |
| D.X和Z的最高价氧化物的水化物都是弱酸 |
对于可逆反应2A(g)+3B(g)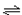 3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是
3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是
A.各物质的量浓度之比为c(A):c(B):c(C)=2:3:3
B.平衡混合物体积是反应开始前的3/5
C.平衡混合物中各物质的量浓度相等
D.单位时间内,若消耗了amolA物质,则同时也消耗了1.5amolC物质
已知强酸与强碱的中和热为57.3kJ/mol,用500mL 0.6mol/L的稀硫酸跟足量的NaOH溶液反应,放出的热量为
| A.68.76 kJ | B.57.3 kJ | C.34.38 kJ | D.17.19 kJ |
在一定条件下,向2L的密闭容器中发生N2+3H2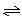 2NH3的反应,自反应开始至2s末,氨的物质的量由0变为0.8 mo
2NH3的反应,自反应开始至2s末,氨的物质的量由0变为0.8 mo l,则以氢气的浓度变化表示该反应在2s内的平均反应速率是
l,则以氢气的浓度变化表示该反应在2s内的平均反应速率是
| A.0.3 mol·L-1 ·s-1 | B.0.4 mol·L-1·s-1 |
| C.0.6 mol·L-1·s-1 | D.0.8 mol·L-1·s-1 |