某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,发生反应:A(g)+B(g)  C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
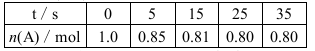
A.反应在前5 s的平均速率v(A)=0.03 mol·L-1·s-1
B.达到平衡时,B的转化率为80%
C.相同温度下,若起始时向容器中充入2.0 mol C,则达到平衡时C的浓度小于0.2 mol·L-1
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆)
标准状况下,某混合物气体由两种气态烃组成,2.24L该混合气体完全燃烧后,得到4.48L二氧化碳和3.6 g水。则这两种气体可能是 ( )
| A.CH4和C3H8 | B.C2H4和C3H4 | C.C2H4和C3H4 | D.C2H2和C2H6 |
某苯的同系物的蒸汽完全燃烧时,需要同条件下12倍于其体积的氧气,则该有机物是()
| A.C8H16 | B.C9H12 | C.C9H14 | D.C10H8 |
某同学写出的下列烷烃的名称中,不正确的是( )
| A.2,3-二甲基丁烷 | B.2,2-二甲基丁烷 |
| C.3-甲基-2-乙基戊烷 | D.2,2,3,3-四甲基丁烷 |
下列叙述错误的是 ( )
| A.在石油分馏和实验室制乙烯装置中,温度计水银球都应放在蒸馏烧瓶支管口附近 |
| B.在石油分馏和实验室制乙烯装置中,反应液都应该加入沸石用来防止暴沸 |
| C.苯可以从煤干馏得到的煤焦油中分离出来,乙烯的工业制法是石油的裂解 |
| D.乙烯实验室制法中,反应液是乙醇和浓硫酸按体积比1∶3配成的,浓硫酸起催化、脱水作用 |
两种气态烃以任意比混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L。下列各组混合烃中不符合此条件的是( )
| A.CH4 C2H4 | B.CH4 C3H4 | C.C2H4 C3H4 | D.C2H2 C3H6 |