下述实验能达到预期目的的是
| 编号 |
实验内容 |
实验目的 |
| A |
向甲苯中滴入少量浓溴水,振荡,静置,溶液分层,下层几乎无色 |
验证甲苯和溴发生取代反应,使溴水褪色 |
| B |
在混有少量苯酚的苯中滴加足量溴水,充分振荡后过滤 |
除去苯中少量的苯酚 |
| C |
溴乙烷与NaOH溶液加热至不再分层,冷却后加稀硝酸至酸性,再滴加AgNO3溶液 |
验证卤素原子为溴 |
| D |
将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 |
检验气体中含有乙烯 |
如下图各烧杯中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
| A.④>②>①>③ | B.②>①>③>④ | C.④>②>③>① | D.③>②>④>① |
在一密闭容器中,反应 aA(g) bB(g)+cC(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则()
bB(g)+cC(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则()
| A.平衡向正反应方向移动了 | B.平衡向逆反应方向移动了 |
| C.物质B的质量分数减小了 | D.a>b+c |
汽车的启动电源常用铅蓄电池,电池反应如下:
PbO2 + Pb + 2H2SO4 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是()
2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是()
| A.PbO2放电时是电池的负极,充电时是电池的阳极。 |
B.负极的电极反应式为:Pb + SO – 2e – = PbSO4 – 2e – = PbSO4 |
| C.放电时,PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
已知热化学方程式:SO2(g)+  O2(g)
O2(g) 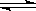 SO3(g)△H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g)△H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
| A.196.64kJ | B.196.64kJ/mol | C.<196.64kJ | D.>196.64kJ |
下列变化属于吸热反应的是 ()
①液态水汽化
②将胆矾加热变为白色粉末
③浓硫酸稀释
④氯酸钾分解制氧气
⑤生石灰跟水反应生成熟石灰
⑥Ba(OH)2·8H2O与NH4Cl晶体混合
| A.①④⑤ | B.①②④ | C.①②⑥ | D.②④⑥ |