化合物C是制备液晶材料的中间体之一,它可由A和B在一定条件下制得
下列说法正确的是
| A.可用FeCl3溶液检验C中是否含有B |
| B.1molC分子最多可与4molH2发生加成反应 |
| C.可以用酸性KMnO4溶液检验B中是否含有-CHO |
| D.1molC与NaOH溶液反应时最多消耗1molNaOH |
一定条件下进行反应:A(g) B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
| t/s |
0 |
2 |
4 |
6 |
8 |
| n(B)/mol |
0 |
0.30 |
0.39 |
0.40 |
0.40 |
下列说法正确的是
A.反应前2min的平均速率v(B)="0.15" mol/(L·min)
B.保持其他条件不变,升高温度,平衡时c(B)="0.22" mol·L-1,则反应的ΔH < 0
C.保持其他条件不变,起始向容器中充入2.0 mol A,反应达到平衡时C的体积分数减小
D.保持其他条件不变,起始向容器中充入1.2 mol A、0.60 mol B和0.60 mol C,反应达到平衡前的速率:v(正)<v(逆)
25℃时,下列有关溶液中微粒的物质的量浓度关系不正确的是
| A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液中:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) |
| B.pH =11的氨水和pH=3的盐酸溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)> c(OH-)>c(H+) |
| C.0.1 mol·L-1 CH3COONa溶液中:c(CH3COO-)+c(CH3COOH) =" 0.1" mol·L-1 |
| D.0.1 mol·L-1的醋酸钠溶液20 mL与0.1 mol·L-1盐酸10 mL混合后溶液显酸性 c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
【原创】下列根据实验操作和现象所得出的结论正确的是:
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
向溶液X中滴加硝酸酸化的Ba(NO3)2溶液 |
产生白色沉淀 |
溶液中一定含有SO42- |
| B |
向溶液X中通入过量二氧化碳气体 |
产生白色沉淀 |
溶液中一定含有SiO32- |
| C |
向溶液X中先滴加稀NaOH溶液,再将湿润蓝色石蕊试纸置于试管口附近 |
试纸不变红 |
原溶液中无NH4+ |
| D |
向溶液X中加入氨水 |
有白色沉淀生成后沉淀不消失 |
溶液X中一定含有Al3+ |
【改编】某有机物的结构简式如图所示,下列有关该物质的叙述正确的是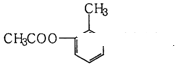
| A.分子中不同化学环境的氢共有4种 |
| B.分子中所有的碳原子不可能共平面 |
| C.能发生取代、消去、加成和氧化反应 |
| D.能使酸性KMnO4溶液褪色 |
下列有关说法正确的是
| A.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
| B.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
C.N2(g)+3H2(g) 2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大 |
| D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的ΔS<0 |