设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,11.2 L乙醇中含有分子的数目为0.5NA |
| B.电解精炼铜的过程中转移了NA个电子,则阴极析出32 g铜 |
| C.2.8 g由氮气和一氧化碳组成的混合气体中含有原子的数目为0.1NA |
| D.加热条件下,20mL 10 mol/L 浓硝酸与足量铜反应转移电子数为0.1NA |
下列表达式错误的是
A.甲烷的电子式: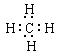 |
| B.乙烯的结构简式为:CH2CH2 |
C.丙烷的球棍模型为: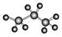 |
D.苯的比例模型为: |
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)
| A.6种 | B.7种 | C.8种 | D.9种 |
下列各组物质不属于同分异构体的是
| A.2,2-二甲基丙醇和2-甲基丁醇 |
| B.邻氯甲苯和对氯甲苯 |
| C.2-甲基丁烷和戊烷 |
| D.乙醇和乙醚 |
有关物质的分类,下列说法正确的是
| A.CH3CH(CH3)2属于链状化合物 | B.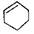 属于芳香族化合物 属于芳香族化合物 |
C. 属于脂环化合物 属于脂环化合物 |
D. 属于芳香烃 属于芳香烃 |
在下列各组物质中,属于同系物的一组是
| A.1,1-二氯乙烷和1,2-二氯乙烷 | B.苯和甲苯 |
| C.乙二醇和丙三醇 | D.乙烯和丙炔 |