氧-18(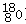 )是氧的一种同位素,称为重氧。最近,兰州近代物理研究所研制出我国首批重氧气,可用符号18O2表示。重氧与普通氢组成的“水”称为重氧水。下列说法正确的是 ( )
)是氧的一种同位素,称为重氧。最近,兰州近代物理研究所研制出我国首批重氧气,可用符号18O2表示。重氧与普通氢组成的“水”称为重氧水。下列说法正确的是 ( )
| A.18g的18O2物质的量是0.1mol |
| B.0.1mol 18O2的体积是2.24L |
| C.18O2气体的摩尔质量是36 |
| D.0.1mol重氧水所含中子数约是6.02×1023个 |
下列有关铁元素的叙述中正确的是( )
| A.Fe(OH)2易被氧化成Fe(OH)3,说明稳定性:Fe(OH)2<Fe(OH)3 |
| B.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| C.氢氧化铁与氢碘酸反应:Fe(OH)3+3HI=FeI3+3H2O |
| D.铁元素位于周期表的第四周期第ⅧB族 |
下列说法正确的是( )
| A.金属钠在空气中燃烧的火焰呈黄色,是因为生成的Na2O2为淡黄色固体 |
| B.铁丝在Cl2中燃烧有红棕色的烟,是因为生成的FeCl3为红棕色固体 |
| C.过量的铁加入稀HNO3,充分反应后,滴入KSCN溶液,溶液呈红色,说明稀HNO3将Fe氧化为Fe3+ |
| D.取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ |
Al、Cu都是重要的金属元素。下列说法正确的是( )
| A.两者对应的氧化物均为碱性氧化物 |
| B.两者的单质都能与稀硫酸反应产生氢气 |
| C.常温条件下,两种金属都能溶解于浓硝酸中 |
| D.制备AlCl3、CuCl2,均不能采用将其溶液直接蒸干的方法 |
下列叙述正确的是( )
| A.金属钠、钾在空气中易被氧化,应该在水中密封保存 |
| B.某气体能使酸性KMnO4溶液褪色,该气体一定是SO2 |
| C.Al(OH)3、NaHCO3和CaCO3均能用来治疗胃酸过多 |
| D.为了延长钢闸门的使用寿命,可将其与电源正极相连 |
下列说法中,正确的是( )
| A.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 |
| B.向氢氧化铁胶体中加入少量稀硫酸,因发生化学反应而产生红褐色沉淀 |
| C.电子工业用30%的氯化铁溶液腐蚀敷在印刷线路板上的铜箔:Fe3++Cu=Fe2++Cu2+ |
| D.Fe分别与少量氯气和稀盐酸反应所得氯化物相同 |