冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或H2或CO)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁。对它们的冶炼方法的分析不正确的是( )
| A.(Ⅰ)用① | B.(Ⅱ)用② | C.(Ⅲ)用③ | D.(Ⅳ)用④ |
2015年8月12日天津港瑞海公司危险化学品仓库发生特大火灾爆炸事故,事故警示我们,化学药品的安全存放是非常重要的。下列有关化学药品的存放说法不正确的是
| A.液溴易挥发,应用少量的水液封并放在冷暗处保存 |
| B.硝酸见光易分解、易挥发,应用棕色广口试剂瓶密封保存 |
| C.金属钠遇到氧气和水均立即反应,应保存在煤油中或者液体石蜡里 |
| D.碳酸钠虽然属于盐,但是其水溶液呈碱性,应用带橡胶塞的试剂瓶保存 |
将KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法正确的是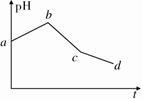
| A.ab段表示电解过程中H+被还原,pH上升 |
| B.电解开始时阳极先发生电极反应2Cl--2e-=Cl2↑ |
| C.电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液 恢复至原来的浓度 |
| D.原混合溶液中KCl和CuSO4的浓度之比恰好为2∶1 |
向盛有 KI 溶液的试管中加入少许 CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色(I2被氧化为 HIO3)。下列说法正确的是
| A.整个过程中的还原剂只有 I2 |
| B.CCl4层由紫色变成无色的化学反应方程式为:I2 + 5Cl2 + 6H2O = 2HIO3 + 10HCl |
| C.若用KI和Cl2反应制 1 mol KIO3,至少需要56 L Cl2(标准状况) |
| D.把 KI 换成 KBr,则 CCl4层变为红棕色。继续滴加氯水,CCl4层的颜色没有变化,则 Cl2、HIO3、HBrO3氧化性由弱到强的顺序是:HBrO3<Cl2<HIO3 |
“暖冰”是韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成的。某老师在课堂上做了一个如右图所示的实验,发现烧杯中溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,则溶液呈血红色。则下列说法中不正确的是
A水凝固形成20~C时的“暖冰”所发生的变化是化学变化
B.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
C.该条件下H2燃烧生成了既具有氧化性又具有还原性的物质
D.该条件下H2燃烧的产物中可能含有一定量的H2O2
某溶液中含K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-中的若干种,某同学欲探究该溶液的组成,进行如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰。
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成。
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色。下列说法正确的是
| A.原溶液中肯定不含Fe2+、NO3-、SiO32-、I- |
| B.原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- |
| C.步骤Ⅱ中无色气体是NO气体,无CO2气体产生 |
| D.为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |