某学习小组同学用右图试剂中的过氧化氢溶液(其中5%为过氧化氢,95%为水)制取氧气,取该溶液17g,加入适量MnO2充分反应。完成下列分析及计算:

(1)小明根据过氧化氢中氧元素的质量分数计算氧气的质量,其计算式为:生成氧气的质量=17g×5%× ×100%=17g×5%×
×100%=17g×5%×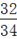 ×100%。
×100%。
老师指出小明的计算是错误的,你认为错误的原因是 (填字母序号)。A.过氧化氢的相对分子质量计算有误 B.过氧化氢中的氧元素没有全部转移到氧气中
(2)请你根据化学方程式计算制取氧气的质量。
取8
氧化铜与100
稀硫酸恰好完全反应后得到蓝色溶液,试计算:
(1)反应后所得溶液中溶质的质量是多少?
(2)求稀硫酸中溶质的质量分数?
二氧化碳是导致温室效应的主要气体,也是一种宝贵的资源,用
和
来合成尿素[
]是固定和利用
的成功范例,其反应的化学方程式为:
请计算下列问题:
(1)若利用
和
生产900
尿素,理论上可固定
的质量是多少吨?
(2)2
含尿素90
的化肥(杂质不含
)中,含氮元素的质量是多少吨?(精确到0.1
).
取一定质量的铜和氧化铜的混合物于烧杯中,向其中加入98g质量分数为10%的稀硫酸,恰好完全反应,得到杯内物质的总质量为118g。求:
(1)原混合物中铜的质量;
(2)反应后所得溶液中溶质的质量分数。(精确到0.1%)
晓东在实验室发现了一瓶敞口放置的过氧化氢溶液,他认为该溶液中溶质的质量分数减小了需要重新测定并更换试剂瓶的标签.他做了如下实验:称量该溶液34.0
倒入烧杯中,然后向其中加入0.4
二氧化锰,直到不再放出气体后,再称量烧杯中混合物的质量,称量结果为33.6
.
(1)生成的气体的质量为;
(2)计算该瓶过氧化氢溶液中溶质的质量分数是多少?
向20g赤铁矿样品中(样品中杂质不溶于水,也不和酸反应)不断加入稀盐酸至固体量不再减少为止,共消耗稀盐酸184g,测得剩余固体的质量为4g。请计算:
(1)赤铁矿样品中,氧化铁的质量分数
(2)最后所得溶液中溶质的质量分数