实验室制取气体所需装置如下所示。请回答以下问题:
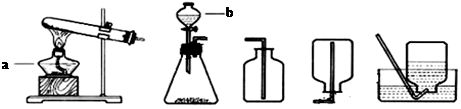
A B C D E
(1)装置中标“a”的仪器名称是 ,标“b”的仪器名称是 。
(2)用高锰酸钾制取并收集一瓶的氧气,发生反应的的符号表达式为 ,所选用的发生装置是 (填字母序号,下同),收集装置是E或 。当用E方法收集O2,收集满并取出集气瓶后,停止该实验的正确操作方法是先 。
(3)利用图Ⅱ装置(夹持装置未画出)能进行的实验是 。
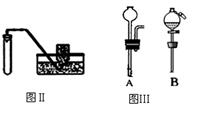
A.用高锰酸钾制氧气
B.用双氧水与二氧化锰制氧气
C.用石灰石与稀盐酸制二氧化碳
(4)图Ⅱ中的气体发生装置虽然简单,操作方便,但无法控制反应速率。请从图III中选取 (选填序号)与图Ⅱ组装成新的气体发生装置,以达到控制反应速率的目的。
(5)催化剂在生产、生活和科研中的地位越来越重要。实验室用过氧化氢溶液分解制取氧气时,就常用二氧化锰作催化剂。
【提出问题】红砖粉能作过氧化氢分解的催化剂吗?
【提出猜想】甲同学认为红砖粉可以代替MnO2作过氧化氢溶液分解的催化剂。
【设计实验】
①在试管中加入10mL6%的过氧化氢溶液,将带火星的木条伸入试管中;
②准确称量0.5g红砖粉,并放入另一支试管中,将带火星的木条伸入试管中;
③在步骤②的试管中加入10mL 6%过氧化氢溶液,将带火星木条伸入试管中;
④待步骤③的试管中无气泡冒出后,经过操作A、洗涤、干燥、称量得粉末仍为0.5g;
⑤另取10mL6%过氧化氢溶液,加入步骤④中所得固体,将带火星木条伸入试管。
【问题讨论】
a.步骤①中的现象为 ,步骤③、⑤中带火星的木条复燃。
b.步骤④中操作A的名称是 。若提供了铁架台、玻璃棒、烧杯还缺少的玻璃仪器为 ,其中玻璃棒的作用为 。
c.步骤①和步骤③的操作目的是 。
d.步骤⑤实验的目的为 。
【实验结论】 。
下图是硫和铁在氧气中燃烧的反应装置图,回答下列问题: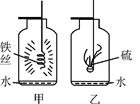
(1)甲、乙两个集气瓶底部的水各有什么作用?
甲:________________________________。
乙:________________________________。
(2)甲、乙两个集气瓶底部的水能否都换成细沙?为什么?
________________________________________________________________________。
根据下列a~e的实验现象,选择最恰当的一项,填入(1)~(4)各相应的反应。
现象:a发出白光;b发出淡蓝色火焰;c发出蓝紫色火焰;
d产生浓厚的白烟;e生成黑色固体
(1)铁丝在氧气中燃烧();
(2)红磷在空气中燃烧();
(3)硫在空气中燃烧()
(2014)小李同学和王老师为探究人体呼出的气体相空气成分的差异.进行的实验如下,小李同学用玻璃管向盛满水的集气瓶中吹气,用排水法收集一瓶呼出的气体,将另一集气瓶充满新鲜的空气,将两根燃着的小木条,分别移到两只集气瓶口处移开玻璃片,慢慢伸入集气瓶中,观察实验现象。王老师将塑料袋内的空气排尽,然后向袋内吹气,收集一定体积的 呼出的气体,利用仪器侧定气体成分(见表1).
表1:室内空气与正常呼吸方式呼出气体中部分气体的含量(体积分数)比较
| 成分 |
室内空气 |
正常呼出的气体 |
变化值 |
| 氧气 |
20.77% |
17.17% |
3.60% |
| 二氧化碳 |
0.056% |
3.67% |
3.6l% |
| 水蒸气 |
1.98% |
2.50% |
0.52% |
(1)人呼出的气体中除含有氧气、二氧化碳、水蒸气外,还含有的主要物质________
(2)小李同学用排水法收集呼出的气体中二氧化碳的量偏小,原因是______________
(3)小李同学进行实验时,发现伸人盛有人呼出气休的集气瓶中燃着的小木条先熄灭其原因可能是_________(写一点即可)
(4)①由表1可知,室内气体与正常呼出的气体相比较,______(填化学式)的含量变化较大,且变化量基本相等。
②人体内的氧气能和许多物质发生反应,写出有机物C6H10O5)和氧气反应,生成二氧化碳和水的化学反应方程式__________________________
通常情况下,空气中各种成分的体积分数是相对稳定的,氮气的体积分数为____ %,氧气约占空气的21%,稀有气体占空气的 %,二氧化碳占0.03%,其他气体和杂质占0.03%。(填气体名称)
下列事实说明空气中含有哪一种成分?,(用化学式填空)
(1)小白鼠放在有空气的密闭容器中可存活一段时间,说明空气中含有 ;
(2)石灰水长期露置于空气中表面有一层白膜,说明空气中含有 ;
(3)薯片露置于空气中逐渐变软,说明空气中含有 ;
(4)豆科植物通过根部的根瘤菌可自己制造氮肥,说明空气中含有 ;
阅读材料,回答问题:
材料1:臭氧是淡蓝色气体,大气中的臭氧层能有效阻挡紫外线,保护地球的生存环境,但目前南极出现了臭氧层空洞,并有继续扩大的趋势。
材料2:复印机在工作时,会因高压放电产生一定浓度的臭氧。长期吸入大量臭氧会引起口干舌燥,咳嗽等不适症状,还可能诱发中毒性肺气肿。
材料3:臭氧发生器是在高压电极的作用下将空气中的氧气转化为臭氧(化学式为O3)的装置。利用臭氧的强氧化性,可将其应用于游泳池、生活用水、污水的杀菌和消毒。
请总结臭氧的有关知识:
(1)物理性质:_____________________________________________________;
(2)化学性质:_________________________________;
(3)用途:_____________________________________________________________;
(4)从上述材料中可见臭氧对人类有利有弊。请再举出一种物质,并说出其利弊:_______________;
(5)请提出一个缩小臭氧层空洞的设想:_____________________________。