苯的同系物C12H18有多种同分异构体,其中二取代苯的同分异构体(不考虑立体异构)有
| A.48种 | B.45种 | C.42种 | D.以上都不是 |
下列离子方程式正确的是()
| A.乙酸与碳酸钠溶液反应:2H++CO32-CO2↑+H2O | ||
| B.甲酸溶液与滴人少量的新制氢氧化铜后共热: △ △ |
C.苯酚钠溶液中通人少量二氧化碳:2C6H5O-+CO2+H2O 2C6H5OH+CO32- 2C6H5OH+CO32- |
D.甲醛溶液与足量的银氨溶液共热: |
HCHO+4[Ag(NH3)2]++4OH CO32-+2NH4++4Ag↓+6NH3+2H2O
CO32-+2NH4++4Ag↓+6NH3+2H2O
下列操作中,完全正确的一组是()
①用试管夹夹持试管叫,试管夹从试管底部上套,夹在试管中上部
②给盛有液体的体积不超过1/3容积的试管加热
③用饱和的Na2CO3溶液除去CO中的CO2
③将试管平放,用纸槽往斌管里送人同体粉末后,然后竖立试管
⑤取用放在细几瓶的液体时,取下瓶塞倒立放在桌面上,倾倒液体时瓶上的标签对着地面
⑥将烧瓶放在桌上,用力塞紧塞子
⑦用坩埚钳夹取加热后的蒸发皿
⑧制取Fe(OH)2时将滴管垂直伸进试管内的液体中
⑨稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑩检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热。
| A.①②④⑦⑧⑩ | B.①④⑤⑦⑨⑩ | C.①④⑤⑦⑧⑩ | D.①②⑤⑦⑨ |
维生素C(Vitamin C)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如右图。下列有关说法中正确的是()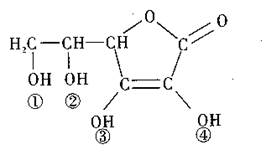 A.维生素C的分子式为C6H 16O6
A.维生素C的分子式为C6H 16O6
B.维生素C 由于含有酯基而难溶于水
C.维生素C由于含有C=O键而能发生
银镜反应
D.维生素C的酸眭可能是③、④两个
羟基引起的
用NA表示阿伏加德罗常数的值,下列说法正确的是()
| A.标准状况下,11.2LNO与5.6LO2混合后的分子总数为0.5NA |
| B.1mol癸烷所含共价键数为29NA |
| C.1mol乙烯基所含电子数为16NA |
| D.乙烯和环丙烷组成的28g混合气体中含有4NA个氢原子 |
将17.9 g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体3.36 L(标准状况)。另取等质量的合金溶于过量的稀硝酸中,生成6.72 LNO(标况),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为()
| A.33.2 g | B.25.4 g | C.22.4 g | D.19.6 g |