如图所示,甲容器容积固定不变,乙容器有可移动的活塞。甲中充入2 mol SO2和1mol O2,乙中充入4 mol SO3和1mol He,在恒定温度和相同的催化剂条件下,发生如下反应:2SO3(g)  2SO2(g)+ O2 (g)。下列有关说法正确的是
2SO2(g)+ O2 (g)。下列有关说法正确的是

| A.若活塞固定在6处不动,达平衡时甲乙两容器中的压强:P乙=P甲 |
| B.若活塞固定在3处不动,达平衡时甲乙两容器中SO3的浓度: c(SO3)乙>2c(SO3)甲 |
| C.若活塞固定在3处不动,达平衡时甲乙容两器中SO2的体积分数:ψ(SO2)乙>2ψ(SO2)甲 |
| D.若活塞固定在7处不动,达平衡时两容器中SO3的物质的量分数相等 |
NF3气体可由氨气和氟气反应得到:4NH3+3F2 = NF3+3NH4F。下列有关说法中正确的是
| A.该反应前后氮元素的化合价不变 |
| B.该反应中的四种物质晶体中都存在氢键 |
| C.该反应中NH3、F2、NF3的分子中所有原子均共平面 |
| D.该反应中NH3、F2、NF3三种物质的晶体均属于分子晶体 |
下列解释实验事实的方程式正确的是
| A.CuSO4溶液中加入过量氨水得到深蓝色溶液:Cu2+ + 2OH-= Cu(OH)2↓ |
B.碳酸钠溶液中滴入酚酞试液,溶液变红:CO32-+ 2H2O  H2CO3 + 2OH- H2CO3 + 2OH- |
| C.FeCl2溶液中加入K3[Fe(CN)6]溶液,生成蓝色沉淀:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓ |
D.90℃时,测得纯水pH =6.7,pH<7的原因是:H2O(l) H+(aq)+ OH-(aq)△H<0 H+(aq)+ OH-(aq)△H<0 |
对下列物质用途的解释中,错误的是
| 选项 |
用途 |
解释 |
| A |
硅胶可作袋装食品的干燥剂 |
硅胶多孔,吸收空气中氧气的能力强 |
| B |
CuSO4可作游泳池的消毒剂 |
铜盐能使构成病毒的蛋白质变性 |
| C |
浸有高锰酸钾溶液的硅藻土可作某些水果的保鲜剂 |
高锰酸钾溶液能氧化水果释放的催熟剂乙烯 |
| D |
Na2O2可作呼吸面具中的供氧剂 |
Na2O2能吸收CO2 同时放出O2 |
下列选项中,为完成相应实验,所用仪器或相关操作合理的是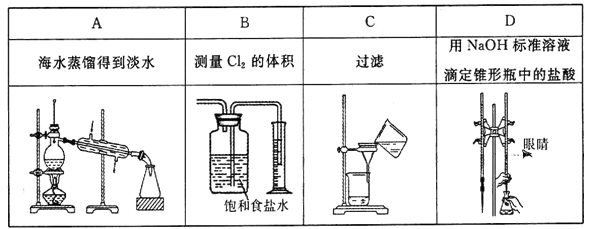
传感器可以检测空气中SO2的含量,传感器工作原理如下图所示。下列叙述中正确的是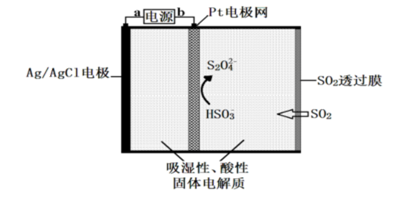
| A.b为电源的正极 |
B.负极反应式 Ag - e- + Cl- 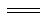 AgCl AgCl |
| C.当电路中电子转移为5×10-5 mol时,进入传感器的SO2为 1.12 mL |
D.阴极的电极反应式是: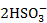 +2H++2e- +2H++2e-  +2H2O +2H2O |