用NA代表阿伏加德罗常数,下列说法正确的是
| A.14g C2H4和C4H8的混合气体中所含的共价键数为3NA |
| B.标准状况下,11.2 L SO3所含的分子数为0.5 NA |
| C.24g 3H218O含有的中子数为12NA |
| D.0.1 mol O22-所含的电子数为1.6NA |
等体积的下列溶液中,阳离子总数最多的是()
| A.0.1mol·L-1的FeCl3溶液 | B.0.1mol·L-1的AlCl3溶液 |
| C.0.05mol·L-1的Na2S溶液 | D.0.05mol·L-1的Al2(SO4)3溶液 |
下列离子因水解相互促进而不能共存的是()
A.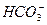 、Na+、Cl-、OH- 、Na+、Cl-、OH- |
B.Al3+、Na+、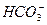 、 、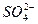 |
C.H+、Fe2+、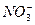 、Cl- 、Cl- |
D.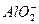 、K+、 、K+、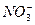 、Al3+ 、Al3+ |
向氨水中逐滴加入稀盐酸,使溶液呈中性,则此时()
A.c(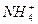 )=c(Cl-) )=c(Cl-) |
B.c(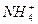 )>c(Cl-) )>c(Cl-) |
C.c(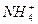 )<c(Cl-) )<c(Cl-) |
D.c(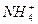 )与c(Cl-)关系不定 )与c(Cl-)关系不定 |
常温下,能使纯水中H+数目增加的是()
| A.S2- | B. |
C. |
D.Br- |
为了使Na2S溶液中c(Na+)/c(S2-)的比值变小,可以加入的物质是()
| A.适量盐酸 | B.适量NaOH溶液 | C.适量KOH溶液 | D.适量KHS溶液 |