某化学兴趣小组将锌片和铜片插入番茄中制成水果电池(如图),下列说法正确的是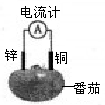
| A.一段时间后,锌片质量会变小 |
| B.铜片上发生氧化反应 |
| C.电子由铜片通过导线流向锌 |
| D.锌电极是该电池的正极 |
下列化学用语正确的是
A.硝基苯的结构简式: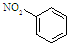 |
B.Be原子的核外电子排布式:1s22s22p1 |
C.氯化铵的电子式: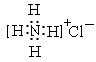 |
D.CO2分子的结构式:O=C=O |
空气是人类生存所必需的重要资源。下列措施不利于改善空气质量的是
| A.燃煤时加适量的生石灰减少二氧化硫的排放 |
| B.实施绿化工程,防治扬尘污染 |
| C.研制开发燃料电池汽车,消除机动车尾气污染 |
| D.加大石油、煤炭的开采速度,增加化石燃料的供应量 |
下列各表述与示意图一致的是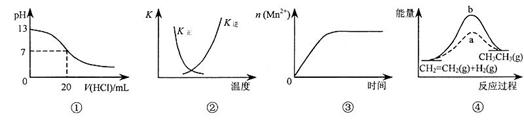
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应2SO2(g)+ O2(g) 2SO3(g)+Q(Q>0)正、逆反应的平衡常数K随温度的变化 2SO3(g)+Q(Q>0)正、逆反应的平衡常数K随温度的变化 |
C.图③表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时(Mn2+是该反应的催化剂),n(Mn2+) 随时间的变化 H2C2O4溶液混合时(Mn2+是该反应的催化剂),n(Mn2+) 随时间的变化 |
D.图④中a 、b曲线分别表示反应CH2=CH2(g)+ H2(g) 、b曲线分别表示反应CH2=CH2(g)+ H2(g) CH3CH3(g) +Q(Q>0),使用和未使用催化剂时,反应过程中的能量变化 CH3CH3(g) +Q(Q>0),使用和未使用催化剂时,反应过程中的能量变化 |
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是()
A.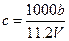 |
B.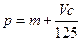 |
| C.n="m+17Vc" | D.p=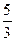 m m |
已知某温度时CH3COOH的电离平衡常数为K。该温度下向20mL0.1mol/LCH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中不正确的是
| A.a 点表示的溶液中c(CH3COO—)=10—3 mol/L |
| B.b 点表示的溶液中c(Na+)> c(CH3COO—) |
| C.c 点表示CH3COOH和NaOH恰好反应完全 |
D.b、d 点表示的溶液中 均等于K 均等于K |