电浮选凝聚法是工业上采用的一种污水处理方法:在污水中通电生成Fe(OH)3胶体,Fe(OH)3胶体可吸附污染物而沉积下来,具有凝聚净化的作用:电极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去浮渣层,即起到了浮选净化的作用。某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法不正确的是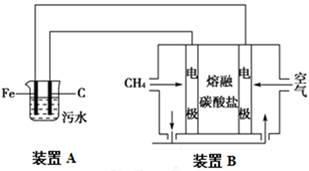
| A.装置A中铁片为阳极,发生的电极反应是Fe-2e- = Fe2+ |
| B.装置B中通入空气的电极反应是O2+2CO2+4e- = 2CO32— |
| C.污水中加入适量的硫酸钠,可增强溶液的导电性,提高污水的处理效果 |
| D.标准状况下,若A装置中产生了44.8L气体,则理论上B装置中要消耗CH4为1.12L |
非金属元素A与金属元素B的离子具有相同电子层结构,原子半径B>A,它们可形成离子化合物B2A,由此下列正确判断是
| A.A可能在第3周期ⅥA族 |
| B.B+离子半径大于A2–离子半径 |
| C.A的电负性大于B的电负性 |
| D.A的第一电离能小于B的第一电离能 |
下列说法正确的是
| A.离子晶体中也可能存在共价键 |
| B.原子晶体中各相邻的原子都以共价键相结合 |
| C.分子晶体的熔沸点较低,常温下都以液体和气体形式存在 |
| D.全由非金属元素形成的化合物一定是共价化合物,属分子晶体 |
现代无机化学对硫—氮化合物的研究是最为活跃的领域之一。其中下图所示是已合成的最著名的硫—氮化合物的分子结构。
下列说法正确的是
| A.该物质的分子式为SN |
| B.该物质的分子中既有极性键,又有非极性键 |
| C.该物质在固态时形成原子晶体 |
| D.该物质与化合物S2N2互为同素异形体 |
高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是
| A.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2— |
| B.晶体中每个K+周围有8个O2—,每个O2—周围有8个K+ |
| C.晶体中与每个K+距离最近的K+有8个 |
| D.晶体中,0价氧原子与-2价氧原子的数目比为3∶1 |
金晶体的晶胞如下图所示立方面心堆积。设金原子的直径为d,用NA表示阿伏加德罗常数,在立方体的各个面的对角线上3个金原子彼此两两相切,M表示金的摩尔质量。则下列说法错误的是
| A.金晶体每个晶胞中含有4个金原子 |
| B.金属键无方向性,金属原子尽可能采取密堆积 |
C.一个晶胞的体积是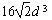 |
D.金晶体的密度是 |