已知25℃时,Ksp(Mg(OH)2)=1.8×10-11,Ksp(Cu(OH)2)=2.2×10-20。请按要求回答下列问题:
(1)在25℃下,向浓度均为0.1 mol・L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成____________沉淀(填化学式),生成该沉淀的离子方程式为________________。
(2)25℃时,向0.01 mol・L-1的MgCl2溶液中,逐滴加入浓NaOH溶液,当Mg2+完全沉淀时,溶液的pH为_______________(忽略溶液体积变化,已知lg1.8=0.26)。
(3)已知25℃时,Ksp(Fe(OH)3)=2.79×10-39,试求该温度下反应Fe(OH)3+3H+ Fe3++3H2O的平衡常数K,写出计算推理过程。
Fe3++3H2O的平衡常数K,写出计算推理过程。
标准状况下CO2和C O的混合气体共17.2 g,总体积为11.2 L,试求该混合气体中CO2和CO的物质的量各为多少。
O的混合气体共17.2 g,总体积为11.2 L,试求该混合气体中CO2和CO的物质的量各为多少。
向50mLNa2SO4和Na2CO3的混合溶液中加入过量BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中再加入过量稀HCl,充分反应后沉淀减少到4.66g,并有气体产生。
⑴求原混合物溶液中Na2SO4和Na2CO3的物质的量。
⑵求产生的气体在标准状况下的体积。
在标准状况下,15g二氧化碳和一氧化碳组成的混合气体,其体积为10.08L,则此混合气体中,一氧化碳和二氧化碳的物质的量之比为多少?
常温下,在27.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为2.0g /cm3,求:
(1)该溶液中阴阳离子的总物质的量
(2)该溶液中CuSO4的物质的量浓度
(3)取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
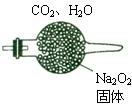
200℃时,11.6gCO2和水蒸气的混合气体与足量的Na2O2充分反应后固体质量增加了3.6g(如图所示),其原混合物中CO2和H2O的物质的量比。