酸根离子RO3-所含电子数比硝酸根离子NO3-的电子数多10,则下列说法正确的是
① R原子的电子层数比N原子的电子层数多1
② RO3-中R元素与 NO3-中N 元素的化合价相同
③ RO3-和NO3-只可能被还原,不可能被氧化
④ R和N不是同周期元素,但为同主族元素
| A.①③④ | B.①②④ | C.①② | D.③④ |
若要检验酒精中是否含有少量水,可选用的试剂是
| A.无水硫酸铜 | B.生石灰 |
| C.浓硫酸 | D.金属钠 |
下列各组给定的物质中,每个原子最外层都满足8电子结构的是
| A.BF3 | B.SO2 | C.PCl3 | D.HClO |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
| A.X、Y、Z的阴离子电子层结构均与R原子的相同 |
| B.常压下,Y单质的沸点比Z单质的沸点高 |
| C.W的氢化物的稳定性比X的氢化物的稳定性强 |
| D.最高价氧化物的水化物酸性W比Y强 |
能说明苯分子中碳碳键不是单、双键相间交替的事实是
①苯不能使酸性KMnO4溶液褪色②苯环中碳碳键均相同
③邻二甲苯只有一种④苯的对位二元取代物只有一种
⑤苯的邻位二氯代物只有一种⑥在一定条件下苯与H2发生加成反应生成环己
| A.①②③④⑤ | B.①②③⑤ |
| C.②③④⑤⑥ | D.①②④⑥ |
某单烯烃经氢化后得到的饱和烃是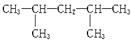 ,该烯烃可能有的结构有
,该烯烃可能有的结构有
| A.1种 | B.2种 | C.3种 | D.4种 |