在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是
A.反应的化学方程式:2N M M |
| B.t2时,正、逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.反应开始时只投入了N |
化学无处不在,与化学有关的说法正确的是
| A.中性溶液的pH都相等 |
| B.新型净水材料高铁酸钠是生产自来水理想的净水剂和杀菌剂 |
| C.127I 和131I2互为同位素 |
| D.ΔH<0,ΔS<0的化学反应不能自发进行 |
相同温度、相同浓度下的六种电解质溶液,其pH由小到大的顺序如图所示,图中:①②③代表的物质可能分别为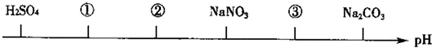
| A.NH4Cl;(NH4)2SO4;CH3COONa | B.(NH4)2SO4;NH4Cl;CH3COONa |
| C.(NH4)2SO4;NH4Cl;NaOH | D.CH3COOH;NH4Cl;(NH4)2SO4 |
可逆反应:2SO2+O2 2SO3的平衡状态下,保持恒温恒容,向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,Qc为浓度商)
2SO3的平衡状态下,保持恒温恒容,向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,Qc为浓度商)
| A.Qc不变,K变大,O2转化率增大 | B.Qc不变,K变大,SO2转化率减小 |
| C.Qc变小,K不变,O2转化率减小 | D.Qc增大,K不变,SO2转化率增大 |
可逆反应:A2(?)+B2(?) 2AB(?);ΔH=-Q kJ/mol,当温度和压强改变时n(AB)的变化如图,下列叙述正确的是
2AB(?);ΔH=-Q kJ/mol,当温度和压强改变时n(AB)的变化如图,下列叙述正确的是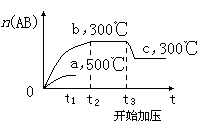
A.A2、B2及AB均为气体,Q>0
B.AB为气体,A2、B2至少有一种为非气体,Q>0
C.AB为气体,A2、B2有一种为非气体,Q<0
D.AB为固体,A2、B2有一种为非气体,Q>0
已知分解1 mol H2O2放出热量 98 KJ,在含少量I-的溶液中,H2O2的分解机理为:
H2O2+ I-→ H2O + IO-(慢); H2O2+ IO-→ H2O + O2+ I-(快)
下列有关反应的说法正确的是
| A.反应的速率与I-的浓度有关 | B.IO-也是该反应的催化剂 |
| C.反应活化能等于98 KJ•mol-1 | D.v(H2O2)=v(H2O)=v(O2) |