根据下列三个方程式:I2+SO2+2H2O=H2SO4+2HI; 2FeCl2+Cl2=2FeCl3;
2FeCl3+2HI=2FeCl2+2HCl+I2 有关微粒的还原性强弱顺序是
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2> I- | C.Fe2+>I->SO2>Cl- | D.SO2>I->Fe2+>Cl- |
在一定条件下,反应N2+3H2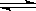 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为
| A.V(NH3)=0.02mol/(L·min) | B.V(N2)=0.005mol/(L·min) |
| C.V(NH3)=0.17mol/(L·min) | D.V(H2)=0.03mol/(L·min) |
下列金属的冶炼不适宜用热还原性来冶炼的是
| A.铁 | B.铜 | C.钠 | D.铅 |
下列有关化学用语表示正确的是
| A.乙酸的结构简式: C2H4O2 | B.F-的结构示意图: |
| C.中子数为20 的氯原子:2017Cl | D.NH3的电子式: |
下列有关实验操作、现象或结论的叙述正确的是
| A.乙醇的催化氧化实验中铜丝主要起氧化剂的作用 |
| B.用钠可以检验某无水酒精中是否含有水 |
| C.制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸 |
| D.除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液 |
下列关于有机物说法正确的是
| A.乙醇、乙烷和乙酸都可以与钠反应生成氢气 |
| B.苯、乙醇和乙酸都能发生取代反应 |
| C.乙醇和乙酸都存在碳氧双键 |
| D.石油分馏可获得乙酸、苯及其衍生物 |