某碳酸钠样品中含有碳酸钾,硝酸钠和硝酸钡三种杂质中的一种或两种。现将11g样品加入足量水中,样品全部溶解。再加入过量的氯化钙溶液,得到10g沉淀。对样品所含杂质的正确判断是
| A.肯定有硝酸钠 |
| B.肯定有硝酸钠,可能还含有碳酸钾 |
| C.肯定没有硝酸钡,可能有硝酸钠 |
| D.肯定没有碳酸钾和硝酸钡 |
浓硫酸具有强烈的吸水性、脱水性与强的氧化性等多重特性,在中学化学实验中经常用浓硫酸制取气体,在以下实验使用的硫酸采用较高浓度的原因不是基于上述特性的是
| A.实验室利用Na2SO3与硫酸制取SO2气体时,一般采用浓度较大的硫酸 |
| B.向白纸上滴几滴浓硫酸 |
| C.向浓硫酸中滴加浓盐酸制取HCl气体 |
| D.利用金属Cu与浓硫酸反应制取SO2气体 |
下列物质能使品红溶液褪色的是
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫 ⑤臭氧
| A.①③④ | B.②④⑤ | C.①②③④ | D.①②③④⑤ |
已知X、Y、Z、W(含同一元素)有如下所示转化关系,且X能与W发生反应生成一种易溶于水的盐,则X可能是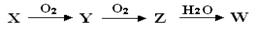
| A.N2 | B.NO2 | C.NH3 | D.NO |
将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→ “出汗” → 变成白色固体(粉末),(银白色→变暗→表面变潮→结块→变成粉末)。下列有关叙述中正确的是
| A.表面迅速变暗是因为钠与空气中的氧气反应生成了过氧化钠 |
| B.“出汗”是因为生成的氢氧化钠吸收空气中的CO2在表面形成了溶液 |
| C.最后变成碳酸钠粉末 |
| D.该过程中的所有化学反应均为氧化还原反应 |
下列除去杂质(括号内的物质为杂质)的方法中错误的是
| A.FeSO4 (CuSO4):加足量铁粉后,过滤 |
| B.CO (CO2):用NaOH溶液洗气后干燥 |
| C.MnO2 (KCl):加水溶解后,过滤、洗涤、烘干 |
| D.CO2 (HCl):用NaOH溶液洗气后干燥 |