氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程示意图如下所示,完成下列填空:
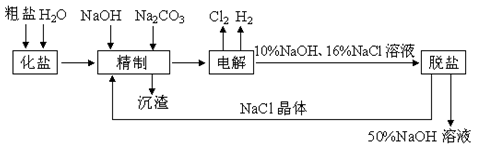

(1)在电解过程中,与电源正极相连的电极上电极反应式为________________,与电源负极相连的电极附近,溶液pH值________(选填“不变”、“升高”或“下降”)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为_________
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是____。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为了有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为____(选填a、b、c)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却结晶、________(填写操作名称)除去NaCl.
已知:H2(g)+ 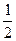 O 2(g)====H2O(g),反应过程中能量变化如下图,问:
O 2(g)====H2O(g),反应过程中能量变化如下图,问:
(1)a、b、c分别代表什么意义?
a._____________________________________________________________________________;
b._____________________________________________________________________________;
c.
_____________________________________________________________________________。
(2)该反应是放热还是吸热?___________。ΔH大于零还是小于零?___________。
科学家预言未来最理想的燃料是绿色植物,即将植物的秸秆[主要成分是纤维素,化学式为(C6H10O5)n],用适当催化剂与水作用生成葡萄糖(分子式为C6H12O6),再在催化剂作用下使葡萄糖分解成乙醇和二氧化碳,乙醇即是一种理想的燃料。试写出两步转化的化学方程式:______________________________、
___________________________________。
(7分)现有下列高聚物:
A.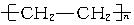 |
B.天然橡胶 | C.硫化橡胶 | D.用于制备电木的酚醛树脂 (E)有机玻璃,其中属于线型结构的是___________,属于体型结构的是___________,可溶于有机溶剂的是___________,加热能熔融的是___________,用于制备轮胎的是___________,用于制备车窗玻璃的是___________,用于制备插座、电器把手的是______________________。 |
(12分)吗啡和海洛因都是严格查禁的毒品。吗啡分子中含C 71.58%、H 6.67%、N 4.91%,其余为O。已知其相对分子质量不超过300,海洛因是吗啡的二乙酸酯。
(1)吗啡的相对分子质量是______________,分子式是____________________________。
(2)海洛因的相对分子质量是_______________,分子式是_________________________。
近来研究认为松果体分泌物——“退黑素”(简称MLT)与人的寿命长短有关,有人把“退黑.素”和克隆技术并称为“20世纪生命科学的两大发现”。“退黑素”的化学结构简式为
(1)“退黑素”的分子式为________________________________________________________。
(2)“退黑素”结构简式中,虚线框内的结构名称为__________________________________,它在稀硫酸中受热后生成的具有酸性的物质为____________________________。