已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:
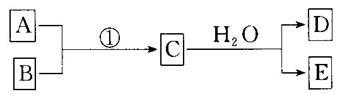
(1)若条件①为常温,B和D为同种无色气体,常温下E的浓溶液可以使Fe钝化,写出少量Fe粉与E的稀溶液反应的离子方程式:_________________________________.
(2)若条件①为加热,E是一种两性氢氧化物,气体D是一种有臭鸡蛋气味的气体,其水溶液是还原性酸,则C为____________(写化学式).
(3)若条件①为点燃,目前60%的B都是从海水中提取的,B常作铝热反应引发剂。气体D可以使湿润的红色石蕊试纸变蓝,写出C与H2O反应的化学方程式__________________。将气体D作为燃料电池的燃料源可以制成D—空气燃料电池系统,总反应式为:D+O2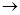 A+H2O(未配平),写出此碱性燃料电池的负极反应式:________________.
A+H2O(未配平),写出此碱性燃料电池的负极反应式:________________.
下图是元素周期表的框架,请在表中①~⑩元素中回答问题
| ① |
|||||||||||||||||
| ② |
③ |
④ |
|||||||||||||||
| ⑤ |
⑥ |
⑦ |
⑧ |
||||||||||||||
| ⑨ |
⑩ |
||||||||||||||||
请用化学语言回答下列问题:
(1)在表中④、⑤、⑥三种元素的简单离子半径由大到小的顺序为__________________________。
(2)其中⑤与⑦两元素的最高价氧化物的水化物反应的离子方程式为_______________________。
(3)⑧与⑩两种元素非金属较强的是________,请用一个离子方程式证明该结论_________。
(4)①与③的两种单质可以在金属铂做电极时构成一种对环境友好的燃料电池,电解质为⑨的最高价氧化物的水化物,请书写出正极反应式_____________________,电池工作时阴离子定向移动到________极(填正或负)。
(5)元素①与⑧的两种单质在一定条件下可反应生成一种化合物甲,已知下表中的数据是破坏1 mol物质中的化学键所吸收的能量(kJ),则生成1mol甲时释放的能量为____________kJ。
| 化学键 |
Cl2 |
Br2 |
I2 |
HCl |
HBr |
HI |
H2 |
| 能量(kJ) |
243 |
193 |
151 |
432 |
366 |
298 |
436 |
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。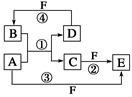
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为________,反应④的化学方程式为___________________________。
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。反应②也在水溶液中进行,其离子方程式是__________________________,
已知光照条件下D与F反应生成B,写出该反应的化学方程式:___________________。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为_____________________________________。
A、B、C、D、E原子序数依次增大, A、B、E的位置如图所示,A、B两种元素的原子序数之和等于E的核电荷数,E原子核内质子数等于中子数; 1molC的单质跟足量盐酸反应,可置换出标准状况下22.4L的H2,这时C转变为与氖原子具有相同电子层结构的离子;在同一周期的元素形成的简单离子中D最小。请回答: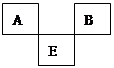
(1)用电子式表示B和C组成的化合物的形成过程为______________________;
(2)D离子的电子式是,A的氢化物的电子式是,E原子的化学符号;
(3)与E同族元素形成的气态氢化物中,沸点最高的是,(填氢化物化学式),原因是;
(4)B、E可能形成EB6型化合物,试从化合价角度说明该化合物能否燃烧。
已知A~O各代表一种物质,除O外其余物质均由短周期元素组成,它们之间的转化关系如下图所示(反应条件略)。A、B、H分别是单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2︰3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。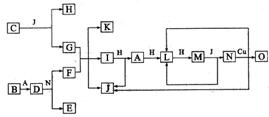
请回答下列问题:
(1)组成B单质的元素位于周期表第周期,第族。化合物C和D的电子式为 ___ 、_____________。
(2)J的沸点比硒化氢(H2Se)的沸点高,其原因是。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:
(4)写出D与足量的N反应生成E和F的化学方程式:。
写出G与F加热反应生成K、I和J的化学方程式:。
(5)上图中在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有个。
A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的―1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题。
(1)B元素在元素周期表中的位置是第______周期______族。
(2)画出D元素的原子结构示意图____________。
(3)与E的氢化物分子所含电子总数相等的分子是____________(举一例、填化学式,下同)、离子是____________。
(4)A与C形成的化合物中含有化学键的类型是____________。
(5)用电子式表示BD的形成过程________________________________