(1)对工业合成氨条件的探索一直是化学工业的重要课题,在恒温恒容的甲容器、恒温恒压的乙容器中分别进行合成氨反应,如下图(图中所示数据均为初始物理量)。t分钟后反应均达到平衡,生成NH3均为0.4mol(忽略水对压强的影响及氨气的溶解)。

①判断甲容器中的反应达平衡的依据是 .(填写相应编号)
| A.压强不随时间改变 |
| B.气体的密度不随时间改变 |
| C.c(N2)不随时间改变 |
| D.单位时间内生成2molNH3的同时消耗1molN2 |
E.单位时间内断裂3 mol H-H键,同时断裂6 mol N-H键
②该条件下甲容器中反应的平衡常数K=
③该条件下,若向乙中继续加入0.2mol N2,达到新平衡时N2转化率= 。
(2)某甲醇(CH3OH)燃料电池原理如图1所示。

①M区发生反应的电极反应式为_______________________________.
②用上述电池做电源,用图2装置电解饱和食盐水(电极均为惰性电极),则该电解池的总反应离子方程式为: . 假设溶液体积为300mL,当溶液的pH值变为13时(在常温下测定),理论上消耗甲醇的质量为______________(忽略溶液体积变化).
写出下列物质的电子式
(1)SiF4
(2)C2H2
(3)NaOH
已知乙烯能发生以下转化:
(1)写出反应的化学方程式
①:反应类型:
②:反应类型:
③:反应类型:_________
(2)丙烯与乙烯的关系是,丙烯发生加聚反应的方程式是_________
下面列出了几组物质,请将物质的合适组号填写在空格上。
同位素,同素异形体,同分异构体。
①刚石与“足球烯”C60;
②D与T;
③16O、17O和18O;
④氧气(O2)与臭氧(O3);
⑤CH4和CH3CH2CH3;
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑦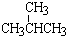 和
和 ;
;
⑧ 和
和  ;
;
写出电极反应式:
(1)钢铁的吸氧腐蚀
正极:;负极:。
(2)氢氧燃料电池(稀硫酸作电解质)
正极:;负极。
热化学方程式:
(1)在标准状况下的11.2L甲烷完全燃烧生成CO2和液态水放出444.8KJ热量(298K),其热化学方程式为。
(2)已知断裂下列1mol化学键需要吸收的能量分别为:C="O:745KJ/mol" , O="O:496kJ/mol" , C-H:414KJ/mol 则断裂1molH-O键需要提供的能量为kJ