已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:
若在反应中消耗了1 mol乙烷(反应物),则有关该反应的说法正确的是
| A.该反应放出251.2 kJ的热量 | B.该反应吸收251.2 kJ的热量 |
| C.该反应放出125.6 kJ的热量 | D.该反应吸收125.6 kJ的热量 |
将0.4 g NaOH和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是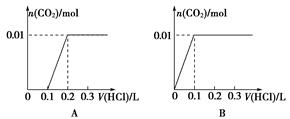
将二氧化硫通入溴水中发生如下的反应:SO2+Br2+2H2O=2HBr+H2SO4,反应中转移的电子数和还原剂是
| A.2e-,H2SO4 | B.4e-,SO2 | C.2e-,Br2 | D.2e-,SO2 |
已知标准状况下:①6.72L CH4②3.01×1023HCl③23.1g CCl4④2.3g Na,下列对四种物质的关系由小到大表示正确的是
| A.体积④<①<②<③ | B.密度①<④<③<② |
| C.原子数④<③<②<① | D.质量④<①<③<② |
下列关于铷的叙述不正确的是
| A.金属铷投入水中会引起爆炸 |
| B.铷是一种强还原剂,铷离子很稳定 |
| C.铷受热后,能在空气中剧烈燃烧,生成比过氧化物更复杂的氧化物 |
| D.铷原子的核电荷数比钾原子的核电荷数多,因此铷原子失电子的能力小于钾原子 |
用NA表示阿伏加德罗常数,下列说法中正确的是
| A.1 mol Al3+含有的核外电子数为3NA |
| B.将58.5 g NaCl溶于1.00 L水中,所得NaCl溶液的浓度为1.00 mol • L−1 |
| C.1 mol Cl2与足量的铁反应,转移的电子数为3NA |
| D.常温下,10L pH=1的硫酸溶液中含有的H+离子数为NA |