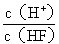下列陈述Ⅰ、Ⅱ正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
浓H2SO4有吸水性 |
浓H2SO4可用于干燥NH3 |
| B |
二氧化硅不与任何酸反应 |
可用石英制造耐酸容器 |
| C |
铝具有强还原性 |
可以通过铝热反应冶炼某些高熔点金属 |
| D |
铜的金属活泼性比铁的弱 |
在海轮外壳上装若干铜块以减缓其腐蚀 |
对于反应A2(g) + 2B2(g)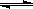 2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是
2AB2(g)(正反应为放热反应),下列各图所表示的变化符合勒夏特列原理的是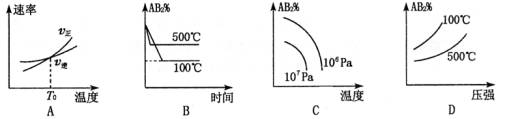
室温时,下列混合溶液的pH一定小于7的是
| A.pH=3的盐酸和pH=11的氨水等体积混合 |
| B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
| C.pH=3的醋酸和pH=11的的氢氧化钡溶液等体积混合 |
| D.pH=3的硫酸和pH=11的氨水等体积混合 |
25℃时,水的电离达到平衡:H2O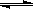 H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
A.向水中加人稀氨水 ,平衡逆向移动,c(OH―)降低 ,平衡逆向移动,c(OH―)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加人少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
取浓度相同的Na0H和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为
| A.0.01mol/L | B.0.017mol/L | C.0.05mol/L | D.0.50mol/L |
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
A. c(H+) B . Ka(HF) C.
. Ka(HF) C.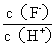 D.
D.