如表所示的四种元素中,W、X、Y、Z均为短周期元素,其中Y是地壳中含量最高的元素,且这四种元素的原子最外层电子数之和为22,下列说法正确的是
| |
X |
Y |
|
| W |
|
|
Z |
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.由X、Z和氢三种元素形成的化合物中只有共价键
C.原子半径的大小顺序:r(X)>r(Y) > r(W) > r(Z)
D.X的最高价氧化物对应的水化物的酸性比W的强
下列有机物分子中,所有原子不可能处在同一平面的是
| A.CH2==="CH—CN" | B.CH≡CH |
C.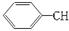 ===CH2 ===CH2 |
D. |
1 mol X能与足量碳酸氢钠溶液反应放出44.8 L CO2(标准状况),则X的分子式是
| A.C5H10O4 | B.C4H8O4 | C.C3H6O4 | D.C2H2O4 |
下列乙醇的化学性质不是由羟基所决定的是
| A.跟金属钠反应 |
| B.在足量氧气中完全燃烧生成CO2和H2O |
| C.在浓H2SO4存在时发生消去反应,生成乙烯 |
| D.当银或铜存在时跟O2发生反应,生成乙醛和水 |
下列事故处理正确的是
| A.苯酚沾在手上立即用水洗涤 |
| B.鱼、肉等食品用福尔马林浸泡防腐保鲜 |
| C.误食铜盐立即喝牛奶或蛋清 |
D.皮肤沾上了浓HNO3而变黄色 ,立即用饱和Na2CO3溶液冲洗 ,立即用饱和Na2CO3溶液冲洗 |
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是
| A.1 mol碳正离子(CH+ 3)所含的电子总数为8NA |
| B.1 mol甲基(—CH3)所含的电子总数为9NA |
| C.0.5 mol 1, 3-丁二烯分子中含有C=C双键数为 NA |
| D.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为7/22.4NA |