实验题:
I.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:
Cl2+2KI===2KCl+I2。请回答下列问题:
(1)指出提取碘的过程中有关实验操作①、③的名称:________;________。
(2)在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是________。(注:如图试管中深色区为紫红色溶液)
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出如图实验装置中的错误之处。(加热装置烧杯下已垫石棉网)
①________________________________________________;
②________________________________________________。
II.某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 |
溶液中检测出的物质 |
| 第一次 |
KCl、K2SO4、Na2CO3、NaCl |
| 第二次 |
KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 |
Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第________次检测结果肯定不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的①________溶液(填化学式),其目的是检验CO32-并将其除去;
第二步:加入②________溶液(填化学式),其目的是③_________________________
________________________________________________________________________;
第三步:过滤,再向滤液中加入④________溶液(填化学式),其目的是⑤________________。
12.4gNa2X中含Na+0.4mol,则Na2X的摩尔质量是,X的相对原子质量是。
过氧化氢(H2O2)有广泛的用途。工业上用电解硫酸氢铵水溶液的方法制备过氧化氢,其反应原理是:2NH4HSO4 (NH4)2S2O8+H2↑,
(NH4)2S2O8+H2↑,
(NH4)2S2O8+2H2O==2NH4HSO4 + H2O2。其流程如下:
回答下列问题:
(1)根据以上反应原理可知,电解硫酸氢铵溶液时,阴极的电极反应方程式是:
。
(2)在上流程图中,采用减压蒸馏的原因是:。
可循环利用的物质是。
(3)过氧化氢具有的化学性质是。
| A.不稳定性 | B.弱碱性 | C.氧化性 | D.还原性 |
(4)硫酸铜溶液中混有少量硫酸亚铁。在除去杂质的过程中,使用过氧化氢时反应的离子方程式是_________________________________________________。
(5)在硫酸的存在下,用过氧化氢与乙酸作用制备过氧乙酸(CH3COOOH)的化学方程式是:_______________________________________________________。
香豆素是用途广泛的香料,合成香豆素的路线如下(其他试剂、产物及反应条件均省略):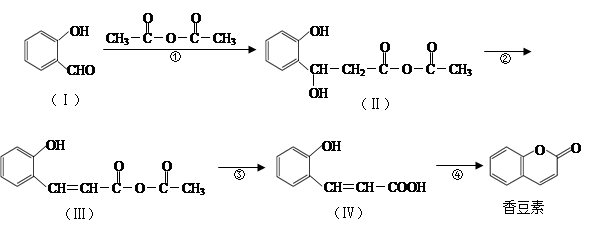
(1)Ⅰ的分子式为_____________;Ⅰ与H2反应生成邻羟基苯甲醇,邻羟基苯甲醇的结构简式为_______ _______。
(2)反应②的反应类型是__________,反应④的反应类型是____________。
(3)香豆素在过量NaOH溶液中完全水解的化学方程式为:
_______________。
(4)Ⅴ是Ⅳ的同分异构体,Ⅴ的分子中含有苯环且无碳碳双键,苯环上含有两个邻位取代基,能发生银镜反应。Ⅴ的结构简式为_______________(任写一种)。
(5)一定条件下,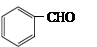 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为_____________。
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为_____________。
(每空2分,共4分).相同条件下,同质量的SO2和SO3气体,体积比为,密度比为
(每空2分,共6分).12.4g Na2R 含有Na+0.4mol,则Na2R的摩尔质量为,R的相对原子质量为,含R1.6g 的Na2R的物质的量为