苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯。

制备苯甲酸苯酯的实验步骤为:
步骤1:将20mL浓H2SO4与40mL冰醋酸在下图装置的烧杯中控制在5℃以下混合。

步骤2:向烧杯中继续加入过硫酸钾25g,用电磁搅拌器搅拌4~5分钟,将二苯甲酮9.1g溶于三氯甲烷后,加到上述混合液中,控制温度不超过15℃,此时液体呈黄色。
步骤3:向黄色液体中加水,直至液体黄色消失,但加水量一般不超过1mL,室温搅拌5h。
步骤4:将反应后的混合液倒入冰水中,析出苯甲酸苯酯,抽滤产品,用无水乙醇洗涤,干燥
(1)步骤1中控制在5℃以下混合的原因为 。
(2)步骤2中为控制温度不超过15℃,向混合液中加入二苯甲酮的三氯甲烷溶液的方法是 。
(3)步骤3中加水不超过1mL,原因是 。
(4)步骤4中抽滤用到的漏斗名称为 。
(5)整个制备过程中液体混合物会出现褐色固体,原因是 ;除去该固体操作为 。
(10分)由乙烯和其它无机原料合成环状化合物E,请在下列图信回答下列问题:
(1)写出①的反应类型②反应条件
(2)B的结构简式 D的结构简式
D的结构简式
(3)E与氢氧化钠溶液反应的化学方程式 .
(1)决定有机物的化学特性的原子或原子团叫做,醇的官能团是(填名称),羧酸的官能团是(填结构简式)。
(2)现有九种有机物:①乙醇② 甲苯③苯酚④甘油⑤甲烷⑥甲醛⑦甲酸⑧乙烯⑨乙炔,将序号填入下列相应的空格中:
甲苯③苯酚④甘油⑤甲烷⑥甲醛⑦甲酸⑧乙烯⑨乙炔,将序号填入下列相应的空格中:
可以作为制取炸药原料的是________(至少写一种);常温下能与溴水发生取代反应的是_________;与溴水发生加成反应的是___________.
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如下图所示,则上述CO2转化为甲醇的反应的△H3_______0(填“>”、“<”或“=”)。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。下列说法正确的是__________(填字母代号)。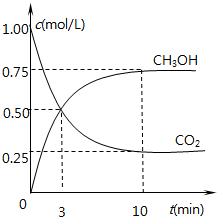
| A.第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时c(CH3OH)=1.5 mol·L-1 |
| B.0-10 min内,氢气的平均反应速率为0.075 mol/(L·min) |
| C.达到平衡时,氢气的转化率为0.75 |
| D.该温度下,反应的平衡常数的值为3/16 |
E.升高温度将使n(CH3OH)/n(CO2)减小
③甲醇燃料电池结构如下图所示。其工作时正极的电极反应式可表示为。
(3)硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为:__________;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na+)+c(H+)__________c(NO3-)+c(OH-)(填写“>”“=”或“<”)
⑴课本设计了如图一所示实验,其目的是通过比较H2O2的分解速率来比较,可通过观察来定性比 较。有同学提出将CuSO4改为CuCl2更为合理,其理由是。
较。有同学提出将CuSO4改为CuCl2更为合理,其理由是。
⑵已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。①针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_____的影响。②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是_____
| A.硫酸钾 | B.硫酸锰 | C.水 | D.氯化锰 |
甲、乙两池电极材料如图所示,请按要求回答下列问题:
|