Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。Q元素的原子最外层电子数是其内层电子数的2倍。W、Z最外层电子数相同,Z的核电荷数是W的2倍。元素Y的合金是日常生活中常用的金属材料。下列说法正确的是
| A.原子半径的大小顺序:rX> rY> rW> rQ |
| B.元素Q和Z能形成QZ2型的共价化合物 |
| C.工业上常用电解的方法制备X、Y的单质 |
| D.X、Y的最高价氧化物的水化物之间不能反应 |
在下列实验中,所选用的仪器合理的是
| A.用50 mL量筒量取5.2 mL稀硫酸 |
| B.用坩埚加热氯化钠溶液得到到氯化钠晶体 |
| C.用托盘天平称量1.17g氯化钠晶体 |
| D.用250 mL容量瓶配制250 mL 0.2 mol/L的NaOH溶液 |
学习化学过程中需要经常做实验。下列实验操作正确的是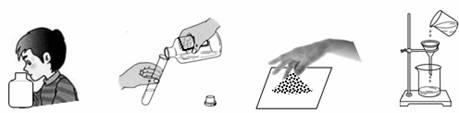
| A.闻气味 | B.倾倒液体 | C.取粉末 | D.过滤 |
下列表示溶液中所发生反应的离子方程式正确的是
A.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH- NH3↑+ H2O NH3↑+ H2O |
| B.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| C.KI溶液与H2SO4酸化的H2O2溶液混合:2I-+ H2O2 + 2H+ =2H2O + I2 |
| D.向氯化银悬浊液中加入饱和碘化钾溶液:Ag+ +I-=AgI ↓ |
NA表示阿佛加德罗常数,下列说法正确的是
| A.0.1molFe与0.1molCl2充分反应转移电子数为0.2NA |
| B.16g甲基正离子(13CH3+)所含中子数为9NA |
| C.关于反应:C2H2(g)+2.5O2(g)= 2CO2(g)+H2O(1)+1300kJ,若CO2中有4NA对共用电子对生成,则放出热量为1300kJ |
| D.0.lmol/L Fe2(SO4)3溶液200mL中阴离子和阳离子总数为0.1NA |
下列离子方程式正确的是
| A.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| B.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-=CO2↑+H2O |
| C.向FeCl3溶液中加入铜片:Fe3++Cu=Fe2++Cu2+ |
| D.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32- |