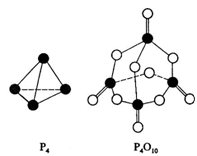
白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P a kJ·mol—1、P—O b kJ·mol—1、P="O" c kJ·mol—1、O="O" d kJ·mol—1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是:
| A.(4a+5d-4c-12b)kJ·mol—1 |
| B.(4c+12b-4a-5d)kJ·mol—1 |
| C.(4c+12b-6a-5d)kJ·mol—1 |
| D.(6a+5d-4c-12b)kJ·mol—1 |
A+B→X+Y+H2O(为配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,该反应的化学方程式是.
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是.
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中.
①A元素在周期表中的位置是______(填所在周期和族);Y的化学式是______.
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是______ mol.
(4)若A、B、X、Y均为化合物.A溶于水电离出的阳离子和水作用的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色.则向A中逐滴加入B的离子方程式为
现将1mo1Cu2S与144克FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2、CuSO4的混合溶液,并产生NO气体。则最终反应所得NO物质的量为
| A.4 mo1 | B.5 mo1 | C.6 mo1 | D.7 mo1 |
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3 +3ClO—+4OH—=2FeO42—+3Cl—+5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
则下列有关说法不正确的是
| A.高铁酸钠中铁显+6价 |
| B.湿法中FeO42—是氧化产物 |
| C.干法中每生成1mol Na2FeO4转移4mol电子 |
| D.K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质 |
学家研制出多种新型杀虫剂代替DDT,化合物M是其中的一种。下列关于M的说法错误的是
| A.M的分子式为C15H22O3 |
| B.与FeCl3溶液发生反应后溶液不显紫色 |
| C.M可以发生银镜反应 |
| D.1molM最多与1molH2完全加成 |
X、Y、Z是位于不同周期的三种短周期元素,且原子序数逐渐增大,X、Z属于同一主族,三种元素可以形成原子个数比为1:1:1的化合物W。下列推测正确的是
| A.元素Z的氧化物一定属于碱性氧化物 |
| B.原子半径关系是:X<Y<Z |
| C.三种元素中,Y的金属性最强 |
| D.Y、Z都能形成含氧酸,且前者的酸性比后者酸性强 |