有机物A由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
(1)有机物A的相对分子质量为 |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次通过碱石灰、无水硫酸铜粉末、足量石灰水,发现碱石灰增重14.2g,硫酸铜粉末没有变蓝,石灰水中有10.0g白色沉淀生成;向增重的碱石灰中加入足量盐酸后,产生4.48L无色无味气体(标准状况)。 |
(2)9.0g有机物A完全燃烧时,经计算: 生成CO2共为 mol, 生成的H2O g, 有机物A的分子式 。 |
| (3)经红外光谱测定,证实其中含有-OH键,-COOH基团,C-H键;其核磁共振氢谱有四组峰,面积比为1﹕3﹕1﹕1。 |
(3)A的结构简式 |
| (4)经红外光谱测定,A的一种同分异构体中,存在-OH键,还含有醛基,C-O键;其核磁共振氢谱有五组峰,面积比为1﹕2﹕1﹕1﹕1。 |
(4)A的同分异构体的 结构简式 |
| (5)如果经红外光谱测定,A的一种同分异构体中,存在-OH键,还含有C=O,C-O键;其核磁共振氢谱有两组峰,面积比为1﹕2。 |
(5)A的同分异构体的 结构简式 |
已知: 。
。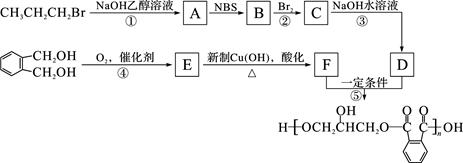
醇酸树脂是一种成膜性良好的树脂,下面是一种醇酸树脂的合成线路:
(1)B中含碳官能团的结构式为_____,C的名称是_____。
(2)反应①的有机反应类型是_____。
(3)下列说法正确的是_____(填字母编号)。
a.1 mol E与足量的银氨溶液反应能生成2 mol Ag
b.F能与NaHCO3反应产生CO2
c.检验CH3CH2CH2Br中的溴原子时,所加试剂的顺序依次是过量氢氧化钠溶液、硝酸银溶液
(4)写出E与新制的氢氧化铜悬浊液反应的化学方程式_____;
(5) 的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
的同分异构体中同时符合下列条件的芳香族化合物共有_____种。
a.能发生消去反应b.能与过量浓溴水反应生成白色沉淀
(6)写出反应⑤的化学方程式_____。
有机化学反应因反应条件不同,可生成不同的有机产品。例如:
HX + 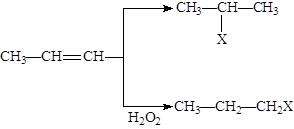 (X为卤素原子)
(X为卤素原子)
工业上利用上述信息,按下列路线合成结构简式为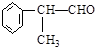 的物质,该物质是一种香料。
的物质,该物质是一种香料。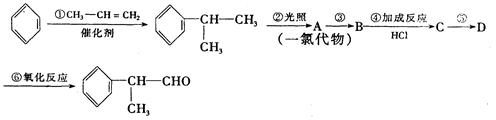
请根据上述路线,回答下列问题:
(1)A的结构简式可能为____________________________________。
(2)反应①、③、⑤的反应类型分别为________、________、_______。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是_______________________________________。
(5)这种香料具有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色 ②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写两种):_____________________________,_______________________________。
(14分)1912年的诺贝尔化学奖授予法国化学家V.Grignard,用于表彰他所发明的Grignard试剂(卤代烃基镁)广泛运用于有机合成中的巨大贡献。Grignard试剂的合成方法是:RX+Mg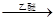 RMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
RMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇: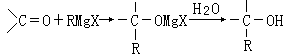
现以2-丁烯和必要的无机物为原料合成3,4-二甲基-3-己醇,进而合成一种分子式为C10H16O4的六元环的物质J,该物质具有一定的对称性,合成线路如下: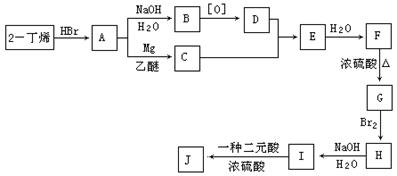
请按要求填空:
(1)3,4-二甲基-3-己醇是:(填代号),E的结构简式是;
(2)C→E的反应类型是,F→G的反应类型是;
(3)写出下列化学反应方程式(有机物请用结构简式表示):
A→B,
B→D,
F→G。
(16分)已知一个碳原子连两个—OH的结构不稳定,会很快脱去一分子水,其变化如下: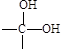 →
→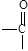 + H2O
+ H2O
下图中B和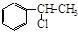 、
、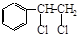 等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳。过程中一些小分子都已经略去。
等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳。过程中一些小分子都已经略去。
(1)A的化学名称为___ _
(2)第④步的化学方程式为__________,该反应类型为_____;
(3)第⑦步的化学方程式为__________,该反应类型为_____;
(4)E的结构简式为______;
(5)符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢的C的同分异构体的结构简式分别是、、。
【化学——选修5:有机化学基础】肉桂酸甲酯是治疗白癜风的重要药物,也是一种用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。它的分子式为C10H10O2,其结构和性质如表所示:
| 结构 |
分子中只含有一个苯环,苯环上只有一个取代基且无支链,核磁共振氢谱图中有六个吸收峰,峰面积比为1∶2∶2∶1∶1∶3 |
| 性质 |
①能使溴水因发生化学反应而褪色 ②在NaOH溶液中易发生水解反应生成具有剧毒的醇类物质 |
试回答下列问题:
(1)肉桂酸甲酯的结构简式为________。
(2)用芳香烃A为原料合成肉桂酸甲酯G的路线如下:
已知: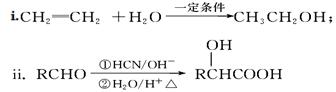
①B的结构简式为________,C中含有的官能团名称为________。
②D→F的反应类型是________;F→G的反应类型是________。
③D转化为F的化学方程式是______________________;
④E为含有三个六元环的酯,其结构简式是_____________________________。
⑤D分子中具有多种官能团,不能发生的反应类型有(填序号)________。
a.酯化反应
b.取代反应
c.加聚反应
d.水解反应
e.消去反应
f.氧化反应
⑥写出符合下列条件的D的同分异构体的结构简式______________________。
i.分子内含苯环,且苯环上只有一个支链;
ii.在催化剂作用下,1 mol该物质与足量氢气充分反应,最多消耗4 mol H2;
iii.它不能发生水解反应。