下图是一个化学过程的示意图。

(1)图中甲池中OH-移向 极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式: 。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为 极(填“A”或"B”),并写出此电极的反应式:____ 。
(4)乙池中总反应的离子方程式:____ 。
(5)当乙池中B(Ag)极的质量增加5.4g时,乙池的pH是 (若此时乙池中溶液的体积为500mlL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是 (填序号)。
| A.MgSO4 | B.CuSO4 | C.AgNO3 | D.AlCl3 |
A、B、C三种元素为短周期元素,A元素的阴离子不能被任何氧化剂氧化,则A离子的结构示意图为___________,它是___________离子。1 mol B单质能从盐酸中置换出3 g氢气,此时B转变为与Ne原子具有相同电子层结构的离子,则B元素是___________;B的最高价氧化物对应水化物的化学式为___________。C元素有3个电子层,且最外电子层比L层少2个电子,则C元素是___________;C与Na反应后生成物的电子式为___________,化合物中的化学键属于___________。
在下列变化中:①I2升华,②烧碱熔化,③NaCl溶于水,④Cl2溶于水,⑤O2溶于水,⑥Na2O2溶于水,以上物质化学键未被破坏的是___________;仅离子键被破坏的是___________;仅共价键被破坏的是___________;离子键被破坏,共价键也被破坏的是___________。
W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中W是原子序数最小的元素,只有Y为金属元素。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。由此可知:
(1)写出元素符号:W为 ,X为 , Y为 ,Z为 。
(2)W2Z是由 键组成的分子,其电子式为 。
(3)由Y、X、W组成的物质中有 键和 键组成的 化合物。
下列结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表代价键(示例F2):  。
。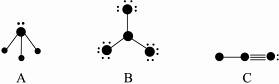
根据各图表示的结构特点,写出各分子的化学式:
A ,B ,C 。
下列五种物质中①Ar②CO2③SiO2④NaOH⑤K2S,只存在共价键的是___________,只存在离子键的是___________,既存在离子键又存在共价键的是___________,不存在化学键的是___________。(填序号)