四种短周期元素在周期表中的相对位置如下所示,其中Z元素最外层电子数是其电子层数的2倍。请回答下列问题:
| X |
Y |
|
| |
Z |
W |
(1)元素Z位于周期表中的位置 。
(2)实验室制取X元素的氢化物的化学方程式为 。
(3)W、Z的最高价氧化物对应的含氧酸的酸性大小顺序 (用化学式表示)。
(4)将W的单质通入含等物质的量FeBr2的溶液中,发生反应的离子方程式为 。
(5)Z和X形成的一种化合物相对分子质量在170~190之间,且Z的质量分数约为70%。该化合物的化学式为 。
如下图所示,甲、乙为相互串联的两电解池。
试回答:
(1)乙池中Fe电极为极。若在乙池中滴入少量酚酞试液,开始电解一段时间后,铁电极附近呈色。
(2)甲池若为精炼铜(假设粗铜的组成是均匀的,且其中活泼和不活泼的成份均存在)的装置,则电解质溶液可以是;通过一段时间后,A电极增重12.8g,则甲池溶液原溶质的浓度(填“增大”、“减小”、“不变”或“无法确定”),乙池石墨电极放出的气体在标准状况下的体积为。
在固定容积的密闭容器中,有可逆反应nA(g)+mB(g) pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值,混合气体的密度;降温时,混合气体的平均相对分子质量;加入催化剂,气体的总物质的量;充入C,则A、B的物质的量。(填增大、减小、不变、不确定)
氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
(2)负极反应式为 。
(3)电极表面镀铂粉的原因为 。
(1)下图表示在密闭容器中反应:2SO2+O2 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是;bc过程中改变的条件可能是;
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是;bc过程中改变的条件可能是;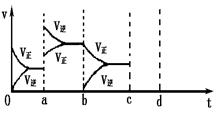
(2)已知下列两个热化学方程式:
H2(g)+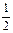 O2(g) = H2O( l )△H=-285.8 kJ·mol-1
O2(g) = H2O( l )△H=-285.8 kJ·mol-1
C3H8(g)+5O2(g) = 3CO2(g) +4H2O(l)△H=-2220.2 kJ·mol-1
实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热3847kJ,则混合气体中H2和C3H8的体积比是
(3)、实验室进行电解氯化钠溶液时,两极共收集到4.48L气体(标况),假设反应后溶液的总体积为200ml,则电解后溶液中氢氧化钠的物质的量浓度
(共10分)某温度时,在2 L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示:
由图中数据分析求:
(1)该反应的化学方程式为。
(2)反应开始 至4 min时,A的平均反应速率为。(要求写出计算过程)
至4 min时,A的平均反应速率为。(要求写出计算过程)
(3)第4min末时A、B的物质的量浓度依次为________、________。第4 min时,正、逆反应速率的大小关系为:v(正)________v(逆)(填“>”、“<”或“=”,下同),第8 min时,v(正)________v(逆)。