已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
请回答下列问题:
(1)B、C、D三种元素的电负性由小到大的顺序为 ,E的基态原子的电子排布式为 。
(2)由B、D形成的BD32-离子中,其VSEPR模型名称是 ,离子的中心原子采用 杂化。
(3)已知由A、C、D三种元素按照4:2:3的原子个数比可形成某离子化合物,常温下测得该离子化合物的水溶液pH=5,则该溶液中水电离出的氢离子浓度为 。
(4) D、E和钡三种元素构成的某化合物的晶胞结构如右图所示,该化合物的化学式为 。

(5)纳米级的EO2是一种广泛使用的催化剂,实验室往往通过ECl4在大量水中加热水解制得EO2·xH2O,该反应的化学方程式为 。
A~H均为短周期元素,A~F在元素周期表中的相对位置如图所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素。由B、G组成的气态化合物甲水溶液呈碱性。
| A |
B |
C |
|
| D |
E |
F |
请回答下列问题:
(1)写出甲的电子式 ,实验室制取气体甲的化学方程式为 。
(2)B、C、G个数比为1:1:5形成的化合物的化学键类型为 。
A.离子键 B. 极性键 C. 非极性键
(3)请用电子式表示AE2的形成过程 。
(4)用离子符号表示C、E、F、H四种离子的半径由大到小的顺序 。
(5)用一个离子方程式解释A比D非金属性强的原因 。
化合物A的分子式为C9H15OCl,分子中含有一个六元环和一个甲基,环上只有一个取代基;F分子中不含甲基:A与其它物质之间的转化如下图所示: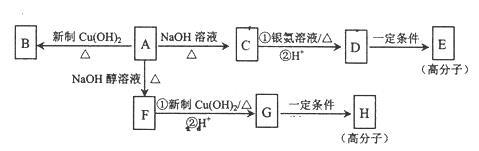
(1) A-F的反应类型是 ;G中含氧官能团的名称是 。
(2) A-C的反应方程式是 。
(3)H的结构简式是 ,E的结构简式是 。
(4)有的同学认为B中可能没有氯原子,你的观点是 (填“同意”或“不同意”)’,你的理由 。
(5某烃的含氧衍生物X符合下列条件的同分异构体中,核磁共振氢谱显示为2组峰的是
(写结构简式);只含有两个甲基的同分异构体有 种。
①相对分子质量比C少54②氧原子数与C相同③能发生水解反应
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下: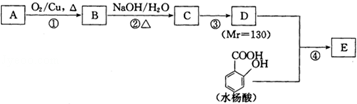
已知:2RCH2CHO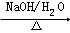
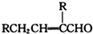
请回答下列问题:
(1)饱和一元醇A中氧的质量分数约为21.6%,则A的分子式为 。结构分析显示A只有一个甲基,则A的名称为 。
(2)B能发生银镜反应,该反应的化学方程式为 。
(3)C中含有官能团的名称为 ;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂 。
(4)第③步的反应类型为 ;D的一种同分异构体M的核磁共振氢谱显示只有一种峰,写出M的结构简式 。
(5)写出E的结构简式 。
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
| 元素编号 |
元素特征信息 |
| A |
A的单质是密度最小的物质 |
| B |
B的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| C |
C的原子最外层电子数是其内层电子数的三倍 |
| D |
D与B同周期,该周期中D的简单离子半径最小 |
| E |
B、C、E组成的36电子的化合物Y是家用消毒剂的主要成分 |
| F |
F元素最高正价与最低负价的代数和为4 |
(1)D的离子结构示意图是___________;化合物Y所含的化学键名称___________;B2C2的电子式表示为 。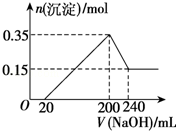
(2)D、E、F的简单离子半径由大到小的顺序是(用化学式表示)________________。
(3)写出两种均含A、B、C、F四种元素的化合物在溶液中相互
反应的离子方程式 。
(4)将一定质量的Mg和D的混合物投入500mL稀硫酸中,
固体全部溶解并产生气体.待反应完全后,向所得溶液中加入
NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中Mg的质量为 ;原稀硫酸溶液的物质的量浓度为 。
某研究小组为了探究固体甲(二元化合物)和固体乙(无机矿物盐,含五种元素)的组成和性质,设计并完成了如下实验: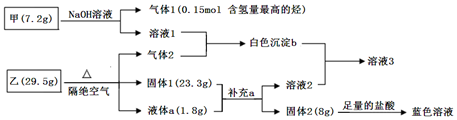
已知:向溶液1中连续滴加盐酸,先产生白色沉淀,后沉淀溶解;向溶液2中连续通入气体2,也是先产生白色沉淀,后沉淀溶解。请回答下列问题:
(1)甲的化学式 ,气体1的结构式 。
(2)加热条件下,气体1与固体2反应,产物中有一种气体和一种固体,该反应的化学方程式为 。
(3)乙的化学式 。
(4)足量气体2与溶液1反应的离子方程式为 。