在氯水中存在多种分子和离子可通过实验的方法加以确定,下列说法中可能错误的是
| A.加入含有NaOH的酚酞试液,红色褪去,说明有H+存在 |
| B.加入有色布条后,有色布条褪色,说明有HClO分子存在 |
| C.氯水呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在 |
| D.加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在 |
下列实验操作能达到实验目的的是
| 选项 |
实验目的 |
实验操作 |
| A. |
除去CO2中的CO |
通过足量的氢氧化钠溶液 |
| B. |
除去NaOH固体中的少量Na2CO3 |
加足量的稀盐酸 |
| C. |
区分NaCl溶液和稀盐酸 |
取样,加入足量NaOH溶液 |
| D. |
区分NaOH溶液和Ca(OH)2溶液 |
取样,分别滴加碳酸钠溶液 |
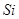 是重要的半导体材料,半导体工业中有一句行话“从沙滩到用户”,指的是利用砂子(主要成分
是重要的半导体材料,半导体工业中有一句行话“从沙滩到用户”,指的是利用砂子(主要成分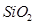 )制取高纯度的
)制取高纯度的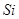 ,其主要化学反应如下:
,其主要化学反应如下:
①2C + SiO2 Si(不纯)+ 2CO↑
Si(不纯)+ 2CO↑
②2Cl2 + Si(不纯) 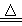 SiCl4
SiCl4
③SiCl4 +2H2 4HCl + Si(高纯)
4HCl + Si(高纯)
下列说法不正确的是
| A.①的目的是将二氧化硅转化成单质硅 |
| B.②③的目的是除去单质硅中混有的杂质 |
| C.上述反应中涉及到2个置换反应 |
| D.上述反应中各元素的化合价都发生了变化 |
下列实验方案能达到实验目的的是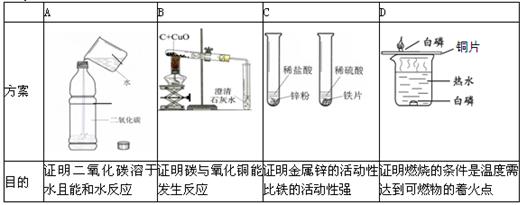
下列说法中,不正确的是
A.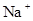 表示钠原子失去1个电子后形成的离子 表示钠原子失去1个电子后形成的离子 |
B.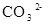 表示带2个单位负电荷的碳酸根离子 表示带2个单位负电荷的碳酸根离子 |
C. 表示氧原子得到1个电子后形成的离子 表示氧原子得到1个电子后形成的离子 |
D. 表示由2个氢原子和2个氧原子构成的过氧化氢分子 表示由2个氢原子和2个氧原子构成的过氧化氢分子 |
以科学原理和实验事实为依据进行推理是学习化学的一种重要方法。下列推理得出的相关结论正确的是
| A.二氧化碳能使燃着木条熄灭,所以能使燃着木条熄灭的气体一定是二氧化碳 |
| B.金刚石与石墨都是由碳元素组成的单质,所以它们的性质完全相同 |
| C.铁丝在氧气中能够燃烧,空气中有氧气,所以铁丝在空气中一定能够燃烧 |
| D.含碳元素的物质充分燃烧会生成CO2,所以燃烧能生成CO2的物质一定含碳元素 |