右图曲线a表示放热反应X(g) + Y(g) 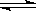 Z(g) + M(g) + N(s) △H <0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g) + M(g) + N(s) △H <0进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
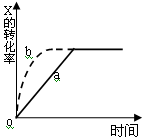
| A.升高温度 | B.加大X的投入量 |
| C.加催化剂 | D.增大体积 |
下列说法不正确的是( )
| A.物质发生化学反应的反应热仅指反应放出的热量 |
| B.热化学方程式中各物质的化学计量数只表示物质的量,不表示分子的个数 |
| C.所有的燃烧反应都是放热的 |
| D.热化学方程式中,化学式前面的化学计量数可以是分数 |
如下图所示曲线a表示放热反应X(g)+Y(g) Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )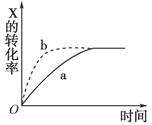
| A.升高温度 | B.加大X的投入量 | C.加催化剂 | D.增大体积 |
下列溶液一定呈中性的是( )
| A.pH=7的溶液 |
| B.c(H+)=c(OH-)的溶液 |
| C.由强酸、强碱等物质的量反应得到的溶液 |
| D.非电解质溶于水得到的溶液 |
参照反应Br+H2―→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )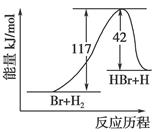
| A.正反应为吸热反应 |
| B.正反应为放热反应 |
| C.加入催化剂,该化学反应的反应热增大 |
| D.从图中可看出,该反应的反应热与反应途径有关 |
可以判定某酸(HA)是强电解质的事实是( )
A.该酸加热至沸腾不分解
B.0.01 mol·L-1该酸的pH=2
C.该酸可以溶解Cu(OH) 2
D.该酸与CaCO3反应放出CO2