下列热化学方程式正确的是
| A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
B.500 ℃、30 MPa 下,将0.5 mol N2和 1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
| C.已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为 H2(g)+ 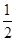 O2(g) O2(g)  H2O(g)ΔH=-242 kJ/mol H2O(g)ΔH=-242 kJ/mol |
| D.25 ℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,硫酸溶液与氢氧化钾溶液反应的热化学方程式为H2SO4(aq)+2KOH(aq)===K2SO4(aq)+2H2O(l) ΔH=-57.3 kJ/mol |
已知H—H键能为436 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2 = 2NH3 ΔH="-92.4" KJ/mol,则N≡N键的键能是
| A.431 KJ/mol | B.946 KJ/mol | C.649 KJ/mol | D.869 KJ/mol |
已知2H2(g)+O2(g) =2H2O(l)ΔH=-569.6kJ/mol,
2H2O(g)=2H2(g)+O2(g) ΔH=+482.1 kJ/mol.
现有1 g液态H2O,蒸发时吸收的热量是
| A.2.43 kJ | B.4.86 kJ | C.43.8 kJ | D.87.5 kJ |
下列各组热化学方程式中,△H1>△H2的是
①C(s)+O2(g)=CO2(g)△H1 C(s)+1/2O2(g)=CO(g)△H2
②S(s)+O2(g)=SO2(g)△H1 S(g)+O2(g)=SO2(g)△H2
③H2(g)+1/2O2(g)=H2O(l)△H1 2H2(g)+O2(g)=2H2O(l)△H2
④CaCO3(s)=CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)=Ca(OH)2(s)△H2
| A.① | B.④ | C.②③④ | D.①②③ |
在进行中和热的测定中,下列操作正确的是
| A.使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差 |
| B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 |
| C.用0.5 mol·L﹣1 NaOH溶液分别与0.5mol·L﹣1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 |
| D.在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计 |
25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g)+O2(g) =2H2O(1)△H= ―285.8kJ/mol |
| B.2H2(g)+ O2(g) =2H2O(1)△H= +571.6 kJ/mol |
| C.2H2(g)+O2(g) =2H2O(g)△H= ―571.6 kJ/mol |
D.H2(g)+ O2(g) =H2O(1)△H= ―285.8kJ/mol O2(g) =H2O(1)△H= ―285.8kJ/mol |