W、X、Y、Z均为短周期元素,原子序数依次增大,Z位于第三周期ⅦA族,且Z比W多11个电子;X、Y原子的核外电子总数为15,X的最高正价与最低负价的代数和为2。下列说法正确的是
| A.原子半径:Y>X |
| B.单质的熔点:X>W |
| C.最简单氢化物的稳定性:Y>W |
| D.最高价氧化物对应水化物的酸性:W>Z |
下列叙述正确的是:
| A.离子化合物中的阴离子肯定不存在金属元素 |
| B.任何的阳离子只有氧化性,任何的阴离子只有还原性 |
| C.与强酸、强碱都会反应的物质中只有两性氧化物或两性氢氧化物 |
| D.根据化合物在水溶液中电离出的离子的类别,将化合物分为酸、碱、盐等 |
下表所列的一些物质或概念间的从属关系中,不符合图示要求的是: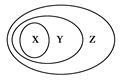
| X |
Y |
Z |
|
| 例 |
氧化物 |
化合物 |
纯净物 |
| A |
碱 |
电解质 |
化合物 |
| B |
胶体 |
分散系 |
混合物 |
| C |
酸性氧化物 |
非金属氧化物 |
化合物 |
| D |
碱性氧化物 |
金属氧化物 |
氧化物 |
下列有关实验操作正确的是: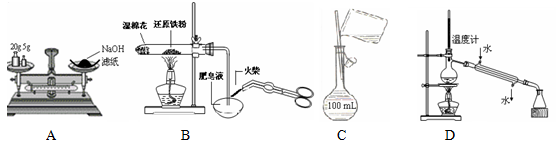
| A.称量氢氧化钠固体 |
| B.检验铁粉与水蒸气反应产生的氢气 |
| C.配制200 mL 0.10 mol · L-1盐酸 |
| D.分离两种互溶但沸点相差较大的液体混合物 |
下列说法正确的是:
| A.执行“限塑令”主要是为了节约资源 |
| B.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| C.利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液 |
| D.工业生产硫酸中,建立高烟囱可以降低地面SO2的浓度,减少空气污染 |
1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(折算到标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2:1 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |