下列对于某些离子的检验说法中正确的是
| A.加入硝酸银产生白色沉淀,一定有Ag+ |
| B.某溶液与NaOH溶液共热,产生使湿润蓝色石蕊试纸变红气体,说明原溶液中存在NH4+ |
| C.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42﹣ |
| D.可用焰色反应实验检验溶液中是否含有K+ |
苯丙酸诺龙是一种兴奋剂,结构简式为: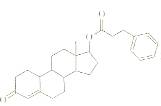 有关该物质的说法正确的是
有关该物质的说法正确的是
| A.其分子式为C27H12O2 | B.最多可与6mol H2发生加成反应 |
| C.能使溴的四氯化碳溶液褪色 | D.在NaOH溶液中水解后可生成两种盐 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是()
| A.2.8g铁粉在1.12L(标准状态)氯气中充分燃烧,失去的电子数为0.15NA |
B.常温下,0.1mol/L HCl溶液中所含的H+个数为0.1NA |
C.26.0g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0 .4NA .4NA |
D.11.2L的CO气体与0.5molN2所含的电子数相等 |
下列装置或操作能达到实验目的是()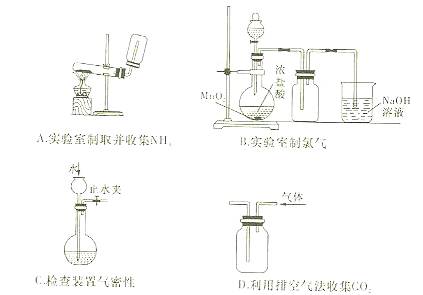
氯所是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是
| A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| B.钠在氯气中燃烧,生成白色的烟 |
| C.纯净的H2在氯气中安静的燃烧,发出苍白色的火焰,集气瓶口呈现白色烟 |
| D.氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
下列对Na2O和Na2O2的叙述中正确的是
| A.Na2O、Na2O2均能与盐酸反应生成NaCl,二者都是碱性氧化物 |
| B.Na2O2在空气中易变质,需要密封保存,Na2O性质稳定,不必密封保存 |
| C.在呼吸面具中,Na2O2能做供氧剂,而Na2O不能 |
| D.将Na2O2放入氢氧化钠溶液中,不发生反应,无明显现象 |