用NA表示阿伏加德罗常数,下列说法正确的是
| A.标准状况下,11.2L H2O所含分子数为0.5NA |
| B.标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA |
| C.1mol·L-1 CaCl2溶液中所含Ca2+离子的数目为NA |
| D.通常状况下,32g O2和O3的混合物所含的氧原子数一定为2NA |
工业上合成氨的原料之一为氢气,其来源之一是利用石油气的有关成分如丙烷(C3H8)制取。以下途径,假设反应都能进行,从经济效益考虑最合理的反应是( )。
A.C3H8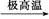 3C+4H2 3C+4H2 |
B.C3H8 C3H6+H2 C3H6+H2 |
C.C3H8+6H2O 3CO2+10H2 3CO2+10H2 |
D.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
下列关于石油、煤、天然气的说法正确的是( )。
| A.石油裂解得到的汽油是纯净物 |
| B.石油产品都可用于聚合反应 |
| C.水煤气是通过煤的液化得到的气体燃料 |
| D.天然气是一种清洁的化石燃料 |
下列金属的冶炼不适宜用热还原法来冶炼的是( )。
| A.铁 | B.铜 | C.钠 | D.铅 |
下列做法能改善空气质量的是( )。
| A.以煤等燃料作为主要生活燃料 |
| B.利用太阳能、风能和氢能等能源代替化石能源 |
| C.鼓励私人购买和使用汽车代替公交车 |
| D.限制使用电动车 |
能源问题是当今世界发展的一个主要问题。下列能源符合“绿色化学”的概念的是( )。
| A.氢气 | B.煤 | C.沼气 | D.石油 |