下列实验操作中正确的是
| A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏时,温度计水银球靠近蒸馏烧瓶的底部 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.检验溶液中是否含有NH4+:取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
把下列四种Na2S2O3溶液分别加入四个盛有10mL 2mol/L硫酸的锥形瓶中,均加水稀释到50mL,其中反应最快的是
| A.10℃,20mL、3mol/L的Na2S2O3溶液 |
| B.20℃,10mL、4mol/L的Na2S2O3溶液 |
| C.20℃,30mL、2mol/L的Na2S2O3溶液 |
| D.10℃,10mL、2mol/L的Na2S2O3溶液 |
可逆反应:3A(g)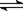 3B(?) + C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是:①B和C可能都是固体 ②B和C一定都是气体 ③若C是固体,则B一定是气体 ④B和C可能都是气体
3B(?) + C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是:①B和C可能都是固体 ②B和C一定都是气体 ③若C是固体,则B一定是气体 ④B和C可能都是气体
| A.①② | B.②③ | C.③④ | D.①④ |
取三张蓝色石蕊试纸置于表面皿上,然后按顺序滴加65%的硝酸,98.3%的硫酸和新制氯水,三张试纸最终呈现的颜色是
| A.白红白 | B.红黑红 | C.红红红 | D.白黑白 |
将等物质的量的X、Y气体充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:X(g)+3Y(g) 2Z(g);△H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2Z(g);△H<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
| 改变条件 |
新平衡与原平衡比较 |
|
| A |
升高温度 |
X的转化率变小 |
| B |
增大压强 |
X的浓度变小 |
| C |
充入一定量Y |
Y的转化率增大 |
| D |
使用适当催化剂 |
X的体积分数变小 |
实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是
| A.CH3COONa固体 | B.NaOH溶液 | C.(NH4)2 SO4粉末 | D.K2 SO4固体 |