如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ中分别加入2 mol X和2 mol Y,开始时容器的体积均为V L,发生如下反应并达到平衡状态: 2X(?)+Y(?) aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是
| A.物质Z的化学计量数a = 2 |
| B.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态 |
| C.若X、Y均为气态,则在平衡时X的转化率:Ⅰ﹤Ⅱ |
| D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ |
相同温度下,下列实验过程中,溶液的浓度和质量始终不变的是
| A.向98.3%浓H2SO4中通入n g SO3 |
| B.向浓氨水中持续通入干燥洁净的空气(已除去(CO2)) |
| C.向KNO3饱和溶液中加入n gKNO3晶体 |
| D.向CuSO4饱和溶液中加入n g无水CuSO4 |
下列各组离子:(1)K+、Fe2+、SO42-、ClO-(2)K+、Al3+、Cl-、HCO3-
(3)ClO-、Cl-、K+、OH- (4)Fe3+、Cu2+、SO42-、Cl-
(5)Na+、K+、AlO2-、HCO3-(6)Ca2+、Na+、SO42-、CO32-
在水溶液中能大量共存的是
| A.(1)和(6) | B.(3)和(4) | C.(2)和(5) | D.(1)和(4) |
下列叙述正确的是
| A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 |
| B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1︰2 |
| C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH |
| D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
下列有关实验的说法正确的是
| A.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 |
| B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 |
| C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中 |
| D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
下列离子方程式不正确的是:
| A.向偏铝酸钠溶液中加入少量的NaHSO4溶液 AlO2- + H+ + H2O = Al(OH)3↓ | |
B.在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解: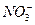 3BaSO3+ 2H+ + 2= 3BaSO4↓ + 2NO↑ + H2O 3BaSO3+ 2H+ + 2= 3BaSO4↓ + 2NO↑ + H2O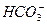 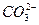 |
C.碳酸钠溶液中通入少量HCl:+ H+ = |
| D.氧化铁可溶于氢碘酸:Fe2O3+ 6H+ = 2Fe3+ + 3H2O |