某气态烃A与H2的相对密度为14,其产量可以用来衡量一个国家的石油化工发展水平。以该化合物为原料合成化合物G、E和I的流程如下:
已知:Ⅰ.芳香族化合物F为C、H、O化合物,其相对分子质量为166,环上的一氯代物有一种,1 mol F与足量NaHCO3溶液反应能生成2 mol CO2,F与足量B反应生成G。
Ⅱ.H为二元醇,其蒸气密度折算成标准状况为2.77 g/L,H与足量D反应生成I。

(1)A 、D分子所含的官能团的名称依次是 、 。
(2)B可以发生的反应有 (选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(3)反应⑤的反应类型为 。
(4)F与H可生成高分子化合物J,写出生成J的化学反应方程式: ,J的名称是 。
(5)写出下列化学方程式:
② ;
⑥ ;
(6) 某学生用新制的Cu(OH)2检验C的官能团,反应的化学方程式为 ,该学生取1mol/LCuSO4溶液和1mol/LNaOH溶液各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL40%的C,加热后无红色沉淀出现。该同学实验失败的原因可能是 。(选填序号)
①加入的C过多 ② 加入的C太少
③ 加入CuSO4溶液的量过多 ④ 加入CuSO4溶液的量不够
(7)I有多种同分异构体,其中一类同分异构体有如下特征:
①分子中含有五元环结构;②1 mol该有机物与足量NaHCO3溶液反应,能生成1 mol CO2;③1 mol该有机物与足量Na反应,能生成1.5 mol H2;④环上的一氯代物只有三种。则满足以上条件的两种有机物的结构简式为: 、
聚己二酸丙二醇酯是性能很好的耐热性和耐久性增塑剂。其中一种合成路线如下:
已知:①烃A的相对分子质量为84,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为一氯代烃;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④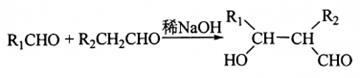 。
。
回答下列问题:
(1)A的结构简式为。
(2)由B生成C的化学方程式为。
(3)由E和F生成G的反应类型为,G的化学名称为 。
(4)①由D和H生成聚已二酸丙二醇酯的化学方程式为。
②若聚已二酸丙二醇酯平均相对分子质量为5600,则其平均聚合度约为(填标号)
a.30 b.35 c.40d.48
(5)D的同分异构体中能同时满足下列条件的共有种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体②既能发生银镜反应,又能发生水解反应。其中核磁共振氢谱显示为4组峰,且峰面积比为6:1:1:2的是(写出其中一种结构简式)。
(6)请设计以甲苯、乙醛为有机原料(其他无机原料任选)合成肉桂酸(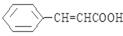 )的合成路线示意图。
)的合成路线示意图。
已知: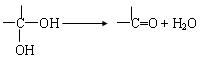
示例: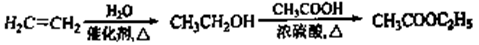
下图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去),已知:a.A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体。b.反应①②是化工生产中的重要反应。c.化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥。d.化合物L具有漂白性,可由Cl2与NaOH溶液反应制得。e.化合物J由两种元素组成,其相对分子质量为32。
请按要求填空:
(1)A元素在元素周期表中的位置____________________。
(2)反应③的化学方程式:________________________。
(3)C的结构式:________;
F的一种用途:_________________________。
(4)L的溶液与化合物E反应的离子方程式:_________ 。
(5)化合物J的化学式: ________________________。
在下图所示的物质转化中,A、C均为常见的金属单质,并且在冷的H的浓溶液中均会发生钝化;E为固体非金属单质。B为红色固体氧化物,X为常见无色液体。L溶液的焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)。
回答以下问题:
(1)H的化学式为。
(2)L的电子式为。
(3)A与B反应的化学方程式为 。
(4)K与足量的氨水反应的离子方程式为 。
乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平。结合以下路线回答:
 已知:CH3CHO + O2
已知:CH3CHO + O2 CH3COOH
CH3COOH
(1)上述过程中属于物理变化的是__________(填序号)。①分馏 ②裂解
(2)A的官能团是__________。
(3)反应II的化学方程式是________________。
(4)D为高分子化合物,可以用来制造多种包装材料,其结构简式是________________。
(5)E是有香味的物质,反应IV的化学方程式是______________________。
(6)下列关于CH2=CH-COOH的说法正确的是__________。
①与CH3CH=CHCOOH互为同系物
②可以与NaHCO3溶液反应放出CO2气体
③在一定条件下可以发生取代、加成、氧化反应
物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A为气体化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。
则
(1)A的分子式是,甲的电子式是。
(2)D的溶液与乙反应的离子方程式是。
(3)若1.7gA与O2反应生成气态的B和C时放出22.67kJ热量,写出该反应的热化学方程式:。