已知:还原性HSO3->I-,氧化性IO3-> I2。在含3 mol NaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和和析出的I2的物质的量的关系曲线如图。下列说法正确的是
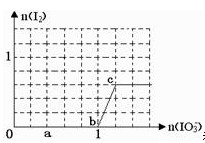
| A.反应过程中的氧化产物均为SO3 |
| B.a点时消耗NaHSO3的物质的量为1.0 mol |
| C.0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+ |
| D.当溶液中I¯与I2的物质的量之比为1:1时,加入的NaIO3为1.2 mol |
下列实验操作与安全事故处理错误的是
| A.使用水银温度计测量烧杯中水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中 |
| B.用试管夹从试管底由下往上夹住距试管口1/3处,手持试管夹长柄末端,进行加热 |
| C.配制少量硫酸溶液时,可先在量筒中加入一定体积水,再在搅拌下慢慢加浓硫酸 |
| D.把玻璃管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻璃管插入端,缓慢旋进塞孔中 |
下列化学用语使用正确的组合是()
①Mg2+结构示意图: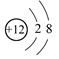 ②乙炔的分子结构模型示意图:
②乙炔的分子结构模型示意图:
③有机还原剂LiAlH4中,氢显-1价④质量数为40的钙原子:
⑤NH4Cl的电子式: ⑥2—甲基丁醇的结构简式:
⑥2—甲基丁醇的结构简式: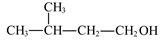
| A.①②③ | B.②④⑤ | C.①③④ | D.①④⑥ |
a1和a2分别为A在两个恒容容器中平衡体系A(g) 2B(g) 和2A(g)
2B(g) 和2A(g) B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是()
B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是()
| A.a1、a2均减小 | B.a1、a2均增大 |
| C.a1增大,a2减小 | D.a1减小,a2增大 |
下列混合溶液中,各离子浓度的大小顺序不正确的是()
| A.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-) + c(CH3COOH)=2c(Na+) |
| B.物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合:离子浓度的大小顺序是: c (Na+)>c (HCO3-)> c(CO32-)>c(OH-)> c(H+) |
| C.0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| D.CH3COONa溶液中c(OH-) = c(CH3COOH) +c(H+) |
下列说法中正确的是()
| A.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均下降 |
| B.常温下,c(NH4+)相等的①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
| C.pH相等的CH3COONa、NaHCO3和Na2CO3三种溶液:c(CH3COONa)<c(NaHCO3) <c(Na2CO3) |
| D.某温度时水的离子积常数KW=10-13若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合,若所得混合液PH=2,则a:b=2:9 |