甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+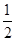 O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
下列说法正确的是( )
| A.CH3OH的燃烧热为192.9 kJ·mol-1 |
B.反应①中的能量变化如下图所示 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
D.根据②推知反应CH3OH(l)+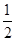 O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 |
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+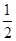 O2(g)ΔH=-266 kJ·mol-1
O2(g)ΔH=-266 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是( )
| A.CO的燃烧热为283 kJ |
| B.右图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g)ΔH>-532kJ·mol-1 |
| D.CO2(g)与Na2O2(s)反应放出532 kJ热量时,转移电子数为6.02×1023 |
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)  2C(g)达到平衡标志的是( )
2C(g)达到平衡标志的是( )
①C的生成速率与C的分解速率相等②单位时间内a mol A生成,同时生成 3amolB③A、B、C的浓度不再变化④混合气体的总压强不再变化⑤混合气体的物质的量不再变化⑥单位时间消耗 a mol A,同时生成3a mol B ⑦A、B、C的分子数目比为1:3:2
A.②④⑤ B.②⑦ C.①③④ D.⑤⑥
在密闭容器中进行下列反应:M(g)+N(g)  R(g)+2X,该反应中R的体积分数如图所示,下列情况正确的是()
R(g)+2X,该反应中R的体积分数如图所示,下列情况正确的是()
| A.正反应为吸热反应,X为气体 |
| B.正反应为吸热反应,X为固体或液体 |
| C.正反应为放热反应,X为气体 |
| D.正反应为放热反应,X为固体或液体 |
下列说法或表示方法中正确的是 ( )
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.由C(金刚石)="==" C(石墨);ΔH="+119" kJ·mol-1可知,石墨比金刚石稳定 |
| C.在101Kpa时,2g H2完全燃烧生成液态水,放出285.8 KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);ΔH=+285.8 kJ·mol-1 |
| D.稀溶液中:H+(aq)+OHˉ(aq)=H2O(l);ΔH=-53.7 kJ·mol-1,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于53.7 kJ |
已知1 g H2完全燃烧生成水蒸气放出热量121 kJ,且O2中1 mol O===O键完全断裂时吸收热量496 kJ,水蒸气中形成1 mol H—O键时放出热量463 kJ,则H2中1 mol H—H键断裂时吸收的热量为
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |