(1)H2SO4的摩尔质量为 ;0.3mol的NH4+中含有 个电子;
(2)①标准状况下22.4 L CH4 ②1.5 mol NH3 ③1.806×1024个H2O ④标准状况下73g HCl所含H原子个数由多到少的顺序为 (填序号);
(3)在含0.4 mol Al2(SO4)3的溶液中SO42-的物质的量为 ;
(4)某常见气体在标准状况下的密度为1.25g/L,若该气体的分子式为A2型,则其名称是 ;
(5)取100 mL a mol / L HCl溶液与300 mL n mol / L H2SO4溶液均注入到500 mL的容量瓶中,加水稀释到刻度线,则该混合溶液中H+ 的物质的量浓度为 mol / L;
我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。某种矿石中铁元素以氧化物FemOn的形式存在,现进行如下实验:将少量铁矿石样品粉碎,称取25.0g样品于烧杯中,加入稀硫酸充分溶解,并不断加热、搅拌,滤去不溶物。向所得滤液中加入10.0g铜粉充分反应后过滤、洗涤、干燥得剩余固体3.6g。剩下滤液用浓度为2mol·L-1的酸性KMnO4滴定,至终点时消耗KMnO4溶液体积25.0mL。
提示:2Fe3++Cu === 2Fe2++Cu2+ 8H++MnO4-+5Fe2+ === Mn2++5Fe3++4H2O
(1)计算该铁矿石中铁元素的质量分数。
(2)计算氧化物FemOn的化学式(m、n为正整数)。
(4分)某同学为了测定镁铝合金中镁的质量分数,取3.9克镁铝合金投入足量的盐酸中,测得生成气体的体积为4.48L(标准状况),请计算该合金中镁的质量分数。(假设合金中不含其它金属)
取1.43g Na2CO3·xH2O 溶于水配成10mL 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸20.0mL,并收集到112mL CO2(标况)。
求:(1)稀盐酸物质的量浓度(2)Na2CO3·xH2O的摩尔质量(3)x值
(12分)向甲乙两个容积均为1 L的恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B。相同条件下(温度T ℃),发生下列反应:A(g)+B(g) xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:
回答下列问题:
(1)乙容器中,平衡后物质B的转化率________;
(2)x=________;
(3)T ℃时该反应的平衡常数为________;
(4)下列说法正确的是________。
A.向平衡后的乙容器中充入氦气可使c(A)增大
B.将乙容器单独升温可使乙容器内各物质的体积分数与甲容器内的相同
C.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol·L-1<c(A)<1.56 mol·L-1
将体积为100 mL浓度为2.0 mol·L־1 的CuSO4溶液和体积为300 mL浓度为1.0 mol·L־1 的H2SO4溶液混合,假定混合后溶液体积为400 mL。计算:
(1)混合液中CuSO4的物质的量浓度是,H2SO4的物质的量浓度是。
(2)往混合液中加水稀释至Cu2+ 浓度为0.2 mol·L־1,则稀释后溶液的体积为。
(3)稀释后溶液中H+ 的物质的量浓度是,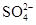 的物质的量浓度是。
的物质的量浓度是。