配制一定物质的量浓度的NaOH溶液时,下列操作会使所配制溶液的浓度偏小的是
①在滤纸上称取NaOH固体;②向容量瓶中转移溶液时有少量溅出;③转移溶液时未洗涤烧杯和玻璃棒;④定容摇匀时液面下降;⑤定容时俯视容量瓶刻度线;⑥定容时仰视容量瓶刻度线
| A.①③④⑤ | B.①②③⑥ | C.②③④⑥ | D.①②④⑤ |
下列有关分子晶体的说法中正确的是( )
| A.分子内均存在共价键 |
| B.分子间一定存在范德华力 |
| C.分子间一定存在氢键 |
| D.其结构一定为分子密堆积 |
下列晶体中的最小环不是由六个原子构成的是( )
| A.金刚石 | B.石墨 | C.水晶 | D.晶体硅 |
制造光导纤维的材料是一种纯度很高的硅氧化物,它是具有立体网状结构的晶体,图3-15是其简化了的平面示意图,下列关于这种材料的说法中正确的是( )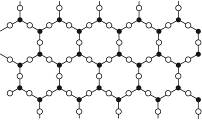
图3-15
| A.晶体中Si与O的数目比是1∶4 |
| B.晶体中Si与O的数目比是1∶6 |
| C.该物质是原子晶体 |
| D.该物质是分子晶体 |
根据下列性质判断,属于原子晶体的物质是( )
| A.熔点2 700 ℃,导电性好,延展性强 |
| B.无色晶体,熔点3 550 ℃,不导电,质硬,难溶于水和有机溶剂 |
| C.无色晶体,能溶于水,质硬而脆,熔点为800 ℃,熔化时能导电 |
| D.熔点-56.6 ℃,微溶于水,硬度小,固态或液态时不导电 |
金刚石是典型的原子晶体,下列关于金刚石的说法中错误的是( )
| A.晶体中不存在独立的“分子” |
| B.碳原子间以共价键相结合 |
| C.是硬度最大的物质之一 |
| D.化学性质稳定,即使在高温下也不会与氧气发生反应 |