一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)  MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )

| 选项 |
x |
y |
| A |
温度 |
容器内混合气体的密度 |
| B |
CO的物质的量 |
CO2与CO的物质的量之比 |
| C |
SO2的浓度 |
平衡常数K |
| D |
MgSO4的质量(忽略体积) |
CO的转化率 |
可逆反应2NO2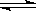 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( )
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2,NO,O2表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②③⑤⑦ | C.①③④⑤ | D.全部 |
把a、b、c、d 4块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,d上产生大量气泡;a、c相连时,电流由c经导线流向a;b、d相连时,电子由d经导线流向b,则此4种金属的活动性由强到弱的顺序为( )
| A.a>b>c>d | B.a>c>d>b | C.c>a>b>d | D.b>a>c>d |
下列说法中正确的是()
| A.在任何物质分子中都含有化学键 |
| B.HF、HCl、HBr、HI的沸点依次升高 |
| C.D2O分子与H2O分子是所含电子总数不相等的分子 |
| D.CO2、PCl3分子中所有原子都满足最外层8电子稳定结构 |
X、Y、Z、W均为短周期元素,它们在周期表中位置如下图所示,若W原子的最外层电子数是内层电子总数的7/10,下列说法中正确的是()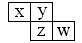
| A.阴离子的半径从大到小排列顺序为:X>Y>Z>W |
| B.Y的两种同素异形体在常温下可以相互转化 |
| C.X、Y两元素的氢化物分子间分别均可以形成氢键 |
| D.最高价氧化物对应的水化物的酸性:Z>W |
下列说法中正确的一组是()
| A.H2和D2互为同位素 |
B.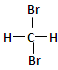 和 和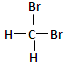 互为同分异构体 互为同分异构体 |
| C.正丁烷和异丁烷是同系物 |
D.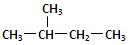 和 和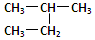 是同一种物质 是同一种物质 |