某同学用中和滴定法测定某烧碱的纯度,实验过程如下:
(1)配制待测液:称取4.1 g固体烧碱样品(杂质不与酸反应)配制成250 mL溶液.
(2)滴定
①用____________量取10.00 mL待测液.
②向锥形瓶中加入几滴酚酞,用0.2010 mol·L-1的标准盐酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,直到______________________时停止滴定.
(3)数据处理
| 实验次 序编号 |
盐酸溶液体积 V/mL |
氢氧化钠溶液体积 V/mL |
| 1 |
19.90 |
10.00 |
| 2 |
20.10 |
10.00 |
| 3 |
22.00 |
10.00 |
| 4 |
20.00 |
10.00 |
根据上述表格,选取合适的数据,计算待测烧碱溶液的浓度为________________,烧碱的纯度为________(保留两位小数)。
(4)一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制盐酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是(多选)( )
A.实验中所用到的滴定管、容量瓶,在使用前均需要检漏
B.如果实验中需用80 mL的稀盐酸标准溶液,配制时应选用100 mL容量瓶
C.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀盐酸,则测得的NaOH溶液的浓度将偏大
E.配制溶液时,定容时俯视读数,则导致实验结果偏大
F.中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大
G.锥形瓶用蒸馏水洗浄后,有少量蒸馏水残留,则导致实验结果偏小
H.滴定前滴定管尖嘴有气泡,滴定后气泡消失,则导致实验结果偏大
(1)下图是一套实验室制取气体的装置,用于发生、干燥和收集气体。下列各组物质中能用这套装置进行实验的是_____________(填编号)。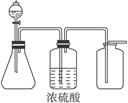
| A.MnO2和浓盐酸 | B.Zn和稀硫酸 |
| C.MnO2和H2O2 | D.CaCO3和盐酸 |
(2)将过氧化氢溶液滴入含有酚酞的氢氧化钠溶液中,红色消失。甲同学认为这是因为过氧化氢是二元弱酸(H2O2 H++
H++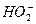 )消耗了OH-,而使酚酞褪色;乙同学认为,过氧化氢具有强氧化性,将酚酞氧化,红色消失。试设计一个简单易行的实验验证甲、乙两同学的解释哪个正确。
)消耗了OH-,而使酚酞褪色;乙同学认为,过氧化氢具有强氧化性,将酚酞氧化,红色消失。试设计一个简单易行的实验验证甲、乙两同学的解释哪个正确。
(3)久置的油画的白色部位(化学成分为PbSO4)常会变黑(化学成分为PbS),用双氧水擦拭后又可恢复原貌,则发生反应的化学方程式为____________________________。
已知硫化氢气体可与溴水反应生成硫,下图是用来制取硫化氢并比较硫元素、溴元素非金属性强弱的实验装置。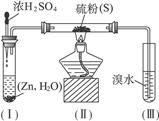
(1)将下列操作步骤补充完整:
①______________________________________________;
②用大火加热使硫沸腾与H2化合;
③______________________________________________;
④停止加热并做善后处理。
(2)装置(Ⅰ)中制氢气不直接用稀硫酸与锌反应,而将浓H2SO4滴入水中,其优点是__________________________________。
(3)装置(Ⅲ)中发生的现象是_______________________________,由此得出的结论是_____________________,反应的离子方程式为____________________________________。
某校开展“研究性学习”中,组织自然科学兴趣小组针对某市热电厂下游境内几十千米内长江中鱼类大量减少的现象,进行了一次调查,并取得了一些资料:
①测定热电厂使用的燃料煤含硫量。测得燃料煤中含硫的质量分数为0.006 4%。
②了解煤燃烧后的气体排放情况。发现:燃烧后的气体未经处理即排放到空气中,该热电厂地处多雨地区。
③了解热电厂发电用水的排放情况。发现:电厂发电用水未经冷却直接排入河中。
根据上述调查资料,完成下列问题:
(1)分析鱼类几近绝迹的原因主要有:
原因一:____________________________________(写化学方程式);
原因二:____________________________________。
(2)项目①中,兴趣小组采用的是_______________分析法。
(3)试计算该热电厂每燃烧1 000 g煤理论上有多少克二氧化硫排放到空气中?
酸雨主要是大量燃烧含硫燃料放出的SO2所造成的。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
| 测定时间/h |
0 |
1 |
2 |
3 |
4 |
| 雨水的pH |
4.73 |
4.62 |
4.56 |
4.55 |
4.55 |
分析数据,完成下列问题:
①雨水样品的pH变化的原因是(用化学方程式表示)________________________________。
②如果将刚取样的上述雨水和自来水混合,pH将变,原因是(用化学方程式表示)_______________________________________________________。
(2)英国的一项研究结果表明:高烟囱可以有效地降低地表面SO2的浓度。在20世纪60—70年代间,由发电厂排出的SO2增加了35%,但由于建筑高烟囱的结果,地面浓度降低了30%之多。请你从全球环境保护的角度,分析这种方法是否可取?简述其理由。
某化学兴趣小组对过量炭粉与氧化铁反应产物中气体的成分进行研究。
(1)假设该反应的气体产物全部是二氧化碳。
(2)设计方案:将一定量氧化铁在隔绝氧气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
(3)查阅资料:氮气不与炭、氧化铁发生反应,可用来隔绝氧气。
(4)实验:
| 操作步骤和实验现象 |
简答 |
| ①称取3.2 g氧化铁与2 g炭粉均匀混合,放入48.48 g的玻璃管中,按上图装置连接 |
①写出装置中编号仪器的名称: A__________,B__________ |
| ②加热前,先通入一定量纯净、干燥的氮气 |
②其目的是_______________ |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 |
③该现象说明__________ |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为52.24 g |
— |
(5)数据处理:经计算,参加反应的碳元素质量为_________g,氧元素质量为____________g。
(6)结论:根据数据处理结果,得出原假设不成立,理由是_____________________________。