下列热化学方程式或离子方程式中,正确的是
| A.氯化镁溶液与氨水反应:Mg2+ + 2OH- = Mg(OH)2 ↓ |
| B.500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: N2(g) + 3H2(g)  2NH3(g)△H= -38.6kJ·mol-1 2NH3(g)△H= -38.6kJ·mol-1 |
| C.甲烷的标准燃烧热△H= -890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g) + 2O2(g) = CO2(g)+2H2O(g) △H= -890.3kJ·mol-1 |
| D.氧化铝溶于NaOH溶液:Al2O3 + 2OH- =2AlO2- + H2O |
下列物质能使干燥的蓝色石蕊试纸变红又褪色的是( )
| A.氯气 | B.液氯 | C.新制氯水 | D.氯气的酒精溶液 |
下列氯化物中不能用金属和氯气直接反应制得的是( )
| A.CuCl2 | B.FeCl2 | C.MgCl2 | D.KCl |
检验SO2气体中是否混有CO2气体,可采用的方法是( )
| A.通过品红溶液 |
| B.通过盐酸,再通过BaCl2溶液 |
| C.先通过NaOH溶液,再通过澄清石灰水 |
| D.先通过酸性KMnO4溶液,再通过澄清石灰水 |
下列离子方程式不正确的是( )
A.石英与烧碱溶液反应:SiO2+2OH-===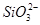 +H2O +H2O |
B.硅与烧碱溶液反应:Si+2OH-+H2O===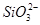 +2H2↑ +2H2↑ |
C.向小苏打溶液中加入过量的石灰水:2HCO+Ca2++2OH-===CaCO3↓+2H2O+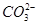 |
D.往水玻璃中加入盐酸:2H++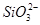 ===H2SiO3↓ ===H2SiO3↓ |
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2: 2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
| A.KClO3在反应中得到电子 | B.ClO2是氧化产物 |
| C.H2C2O4在反应中被还原 | D.1 mol KClO3参加反应有2 mol电子转移 |